
Ionisierende Strahlung ist jede Strahlung ( Partikel oder elektromagnetische Wellen ), die genug Energie enthält, um Elektronen von Atomen oder Molekülen zu stoßen und sie dadurch zu ionisieren. Für ionisierende Strahlung ist die kinetische Energie von Partikeln ( Photonen, Elektronen usw. ) ausreichend und das Partikel kann Zielatome ionisieren (um Ionen durch Elektronenverlust zu bilden), um Ionen zu bilden.
Die Grenze zwischen ionisierender und nichtionisierender Strahlung ist nicht scharf definiert, da unterschiedliche Moleküle und Atome bei unterschiedlichen Energien ionisieren. Dies ist typisch für elektromagnetische Wellen. Zu den elektromagnetischen Wellen gehören in der Reihenfolge zunehmender Frequenz (Energie) und abnehmender Wellenlänge: Radiowellen, Mikrowellen, Infrarotstrahlung, sichtbares Licht, Ultraviolettstrahlung, Röntgenstrahlung und Gammastrahlung. Gammastrahlen , Röntgenstrahlen und der höhere ultraviolette Teil des Spektrums ionisieren, wohingegen das niedrigere ultraviolette, sichtbare Licht (einschließlich Laserlicht), Infrarot, Mikrowellen und Radiowellen als nicht ionisierende Strahlung gelten.
Alle biologischen Schädigungseffekte beginnen mit der Folge von Strahlungswechselwirkungen mit den Atomen, die die Zellen bilden. Alle Lebewesen bestehen aus einer oder mehreren Zellen. Jeder Teil Ihres Körpers besteht aus Zellen oder wurde von ihnen aufgebaut. Obwohl wir die Tendenz haben, biologische Effekte in Bezug auf die Wirkung von Strahlung auf lebende Zellen zu sehen , interagiert ionisierende Strahlung per Definition nur mit Atomen durch einen Prozess, der Ionisation genannt wird.
Die Gefahr ionisierender Strahlung besteht darin, dass die Strahlung unsichtbar ist und von den menschlichen Sinnen nicht direkt wahrgenommen werden kann. Menschen können Strahlung weder sehen noch fühlen, aber sie gibt Energie an die Körpermoleküle ab. Die Energie wird für jede Wechselwirkung zwischen der Strahlung und einem Molekül in kleinen Mengen übertragen, und es gibt gewöhnlich viele solcher Wechselwirkungen.
Formen ionisierender Strahlung
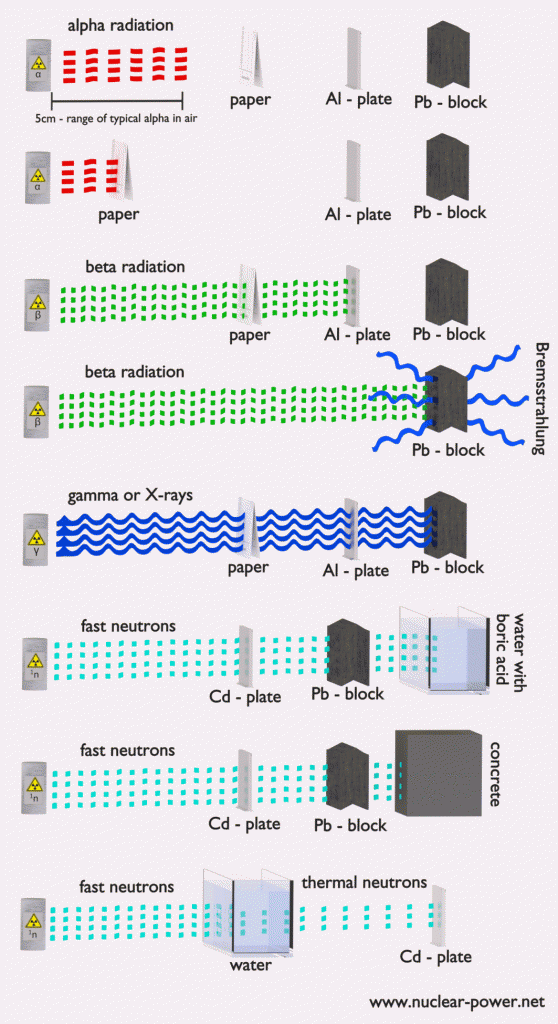 Ionisierende Strahlung wird nach der Art der Partikel oder elektromagnetischen Wellen kategorisiert, die den ionisierenden Effekt erzeugen. Diese Teilchen / Wellen haben unterschiedliche Ionisationsmechanismen und können wie folgt gruppiert werden:
Ionisierende Strahlung wird nach der Art der Partikel oder elektromagnetischen Wellen kategorisiert, die den ionisierenden Effekt erzeugen. Diese Teilchen / Wellen haben unterschiedliche Ionisationsmechanismen und können wie folgt gruppiert werden:
- Direkt ionisierend . Geladene Teilchen ( Atomkerne, Elektronen, Positronen, Protonen, Myonen usw. ) können Atome direkt durch fundamentale Wechselwirkung durch die Coulomb-Kraft ionisieren, wenn sie ausreichend kinetische Energie tragen. Diese Teilchen müssen sich mit relativistischen Geschwindigkeiten bewegen, um die erforderliche kinetische Energie zu erreichen. Sogar Photonen (Gammastrahlen und Röntgenstrahlen) können Atome durch den photoelektrischen Effekt und den Compton-Effekt direkt (obwohl sie elektrisch neutral sind) ionisieren, aber die sekundäre (indirekte) Ionisation ist viel bedeutender.
- Alpha-Strahlung . Alphastrahlung besteht aus Alphateilchen mit hoher Energie / Geschwindigkeit. Die Produktion von Alpha-Partikeln wird als Alpha-Zerfall bezeichnet. Alpha-Teilchen bestehen aus zwei Protonen und zwei Neutronen, die zu einem Teilchen zusammengebunden sind, das mit einem Heliumkern identisch ist. Alpha-Teilchen sind relativ groß und tragen eine doppelt positive Ladung. Sie sind nicht sehr durchdringend und ein Stück Papier kann sie aufhalten. Sie reisen nur wenige Zentimeter, legen aber ihre ganze Energie auf ihren kurzen Wegen ab.
- Beta-Strahlung . Beta-Strahlung besteht aus freien Elektronen oder Positronen mit relativistischen Geschwindigkeiten. Beta-Teilchen (Elektronen) sind viel kleiner als Alpha-Teilchen. Sie tragen eine einzige negative Ladung. Sie sind durchdringender als Alpha-Partikel, aber dünnes Aluminiummetall kann sie aufhalten. Sie können mehrere Meter zurücklegen, aber an jedem Punkt ihrer Wege weniger Energie ablagern als Alpha-Partikel.
- Indirekt ionisierend . Indirekte ionisierende Strahlung besteht aus elektrisch neutralen Partikeln und interagiert daher nicht stark mit Materie. Der Großteil der Ionisationseffekte ist auf Sekundärionisationen zurückzuführen.
- Photonenstrahlung ( Gammastrahlen oder Röntgenstrahlen). Photonenstrahlung besteht aus hochenergetischen Photonen . Diese Photonen sind Teilchen / Wellen (Wellen-Teilchen-Dualität) ohne Ruhemasse oder elektrische Ladung. Sie können 10 Meter oder mehr in der Luft fliegen. Dies ist eine große Entfernung im Vergleich zu Alpha- oder Betateilchen. Gammastrahlen lagern jedoch weniger Energie auf ihren Wegen ab. Blei, Wasser und Beton stoppen die Gammastrahlung. Photonen (Gammastrahlen und Röntgenstrahlen) können Atome direkt durch den photoelektrischen Effekt und den Compton-Effekt ionisieren, wo das relativ energetische Elektron erzeugt wird. Das Sekundärelektron erzeugt weiterhin mehrere Ionisationsereignisse , daher ist die sekundäre (indirekte) Ionisation viel bedeutender.
- Neutronenstrahlung . Neutronenstrahlung besteht aus freien Neutronen bei allen Energien / Geschwindigkeiten. Neutronen können durch Kernspaltung oder durch Zerfall einiger radioaktiver Atome emittiert werden . Neutronen haben keine elektrische Ladung und können keine direkte Ionisation verursachen. Neutronen ionisieren Materie nur indirekt . Wenn beispielsweise Neutronen auf die Wasserstoffkerne treffen, entsteht Protonenstrahlung (schnelle Protonen). Neutronen können von Partikeln mit hoher Geschwindigkeit und hoher Energie bis zu Partikeln mit niedriger Geschwindigkeit und niedriger Energie (sogenannte thermische Neutronen) reichen. Neutronen können sich ohne Wechselwirkung über mehrere hundert Meter in der Luft bewegen.
High-LET- und Low-LET-Strahlung
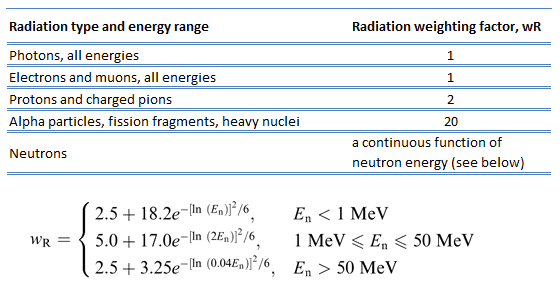
Wie geschrieben wurde, interagiert jede Art von Strahlung auf unterschiedliche Weise mit Materie . Beispielsweise können geladene Teilchen mit hohen Energien Atome direkt ionisieren. Alpha-Partikel sind ziemlich massiv und tragen eine doppelte positive Ladung, so dass sie dazu neigen, sich nur über eine kurze Strecke zu bewegen und nicht oder nur sehr weit in das Gewebe einzudringen. Alpha-Partikel lagern ihre Energie jedoch über ein kleineres Volumen ab (möglicherweise nur wenige Zellen, wenn sie in einen Körper gelangen) und verursachen mehr Schaden an diesen wenigen Zellen.
Beta-Teilchen (Elektronen) sind viel kleiner als Alpha-Teilchen. Sie tragen eine einzige negative Ladung. Sie sind durchdringender als Alpha-Partikel. Sie können mehrere Meter zurücklegen, aber an jedem Punkt ihrer Wege weniger Energie ablagern als Alpha-Partikel. Dies bedeutet, dass Beta-Partikel dazu neigen, mehr Zellen zu schädigen, jedoch jeweils weniger. Andererseits interagieren elektrisch neutrale Teilchen nur indirekt, können aber auch einige oder alle ihrer Energien auf die Materie übertragen.
Es würde sicherlich die Sache vereinfachen, wenn die biologischen Wirkungen der Strahlung direkt proportional zur absorbierten Dosis wären . Leider hängen die biologischen Wirkungen auch davon ab, wie sich die absorbierte Dosis auf dem Strahlungsweg verteilt. Studien haben gezeigt, dass Alpha- und Neutronenstrahlung bei einer bestimmten Energiedeposition pro kg Gewebe einen größeren biologischen Schaden verursachen als Gammastrahlung. Es wurde festgestellt, dass die biologischen Auswirkungen jeglicher Strahlung mit dem linearen Energietransfer (LET) zunehmen . Kurz gesagt, die biologische Schädigung durch Strahlung mit hohem LET ( Alpha-Teilchen , Protonen oder Neutronen)) ist viel größer als die von Low-LET-Strahlung ( Gammastrahlen ). Dies liegt daran, dass das lebende Gewebe Schäden durch Strahlung, die sich über einen großen Bereich ausbreitet, leichter reparieren kann als solche, die sich auf einen kleinen Bereich konzentrieren. Natürlich können Gammastrahlen bei sehr hoher Exposition das Gewebe immer noch stark schädigen.
Da bei gleicher physikalischer Dosis mehr biologische Schäden verursacht werden (dh dieselbe Energie pro Masseeinheit Gewebe), ist ein Grau Alpha- oder Neutronenstrahlung schädlicher als ein Grau Gammastrahlung. Diese Tatsache, dass Strahlungen unterschiedlicher Art (und Energien) unterschiedliche biologische Wirkungen bei gleicher absorbierter Dosis bewirken, wird anhand von Faktoren beschrieben, die als relative biologische Wirksamkeit (RBE) und Strahlungsgewichtungsfaktor (wR) bekannt sind.
Der Strahlungsgewichtungsfaktor ist ein dimensionsloser Faktor, der verwendet wird, um die äquivalente Dosis aus der über ein Gewebe oder Organ gemittelten absorbierten Dosis zu bestimmen, und basiert auf der Art der absorbierten Strahlung. Die resultierende gewichtete Dosis wurde als Organ- oder Gewebeäquivalentdosis bezeichnet:
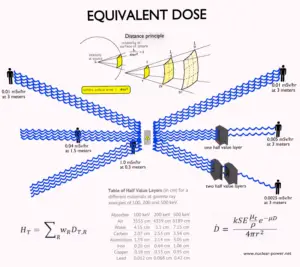 Eine äquivalente Dosis von einem Sievert darstellt , dass die Menge der Strahlungsdosis , die äquivalent ist, in Bezug auf den angegebenen biologischen Schäden , zu einem grauen von Röntgenstrahlen oder Gammastrahlen . Die äquivalente Dosis ist eine nicht physikalische Größe (w R wird aus den biologischen Folgen ionisierender Strahlung abgeleitet), die in der Dosimetrie, gemessen mit Dosimetern, weit verbreitet ist. Die äquivalente Dosis wird vom ICRP als „Grenzmenge“ bezeichnet. Expositionsgrenzwerte festzulegen, um sicherzustellen, dass „das Auftreten stochastischer Auswirkungen auf die Gesundheit unter inakzeptablen Werten gehalten wird und dass Gewebereaktionen vermieden werden“.
Eine äquivalente Dosis von einem Sievert darstellt , dass die Menge der Strahlungsdosis , die äquivalent ist, in Bezug auf den angegebenen biologischen Schäden , zu einem grauen von Röntgenstrahlen oder Gammastrahlen . Die äquivalente Dosis ist eine nicht physikalische Größe (w R wird aus den biologischen Folgen ionisierender Strahlung abgeleitet), die in der Dosimetrie, gemessen mit Dosimetern, weit verbreitet ist. Die äquivalente Dosis wird vom ICRP als „Grenzmenge“ bezeichnet. Expositionsgrenzwerte festzulegen, um sicherzustellen, dass „das Auftreten stochastischer Auswirkungen auf die Gesundheit unter inakzeptablen Werten gehalten wird und dass Gewebereaktionen vermieden werden“.
Ionisationsenergie
Ionisierungsenergie , auch Ionisierungspotential genannt , ist die Energie, die erforderlich ist, um ein Elektron aus dem neutralen Atom zu entfernen .
X + Energie → X + + e –
wobei X ein Atom oder Molekül ist, das ionisiert werden kann, ist X + das Atom oder Molekül, bei dem ein Elektron entfernt ist (positives Ion), und e – ist das entfernte Elektron.
Ein Stickstoffatom benötigt beispielsweise die folgende Ionisierungsenergie, um das äußerste Elektron zu entfernen.
N + IE → N + + e – IE = 14,5 eV
Die mit der Entfernung des ersten Elektrons verbundene Ionisierungsenergie wird am häufigsten verwendet. Die n- te Ionisierungsenergie bezieht sich auf die Energiemenge, die erforderlich ist, um ein Elektron mit einer Ladung von ( n –1) aus der Spezies zu entfernen .
1. Ionisierungsenergie
X → X + + e –
2. Ionisierungsenergie
X + → X 2+ + e –
3. Ionisierungsenergie
X 2+ → X 3+ + e –
Ionisierungsenergie für verschiedene Elemente
Für jedes aufeinanderfolgende entfernte Elektron gibt es eine Ionisierungsenergie. Die Elektronen, die den Kern umkreisen, bewegen sich in ziemlich genau definierten Bahnen. Einige dieser Elektronen sind im Atom fester gebunden als andere. Zum Beispiel sind nur 7,38 eV erforderlich, um das äußerste Elektron von einem Bleiatom zu entfernen, während 88.000 eV erforderlich sind, um das innerste Elektron zu entfernen. Hilft, die Reaktivität von Elementen (insbesondere Metallen, die Elektronen verlieren) zu verstehen.
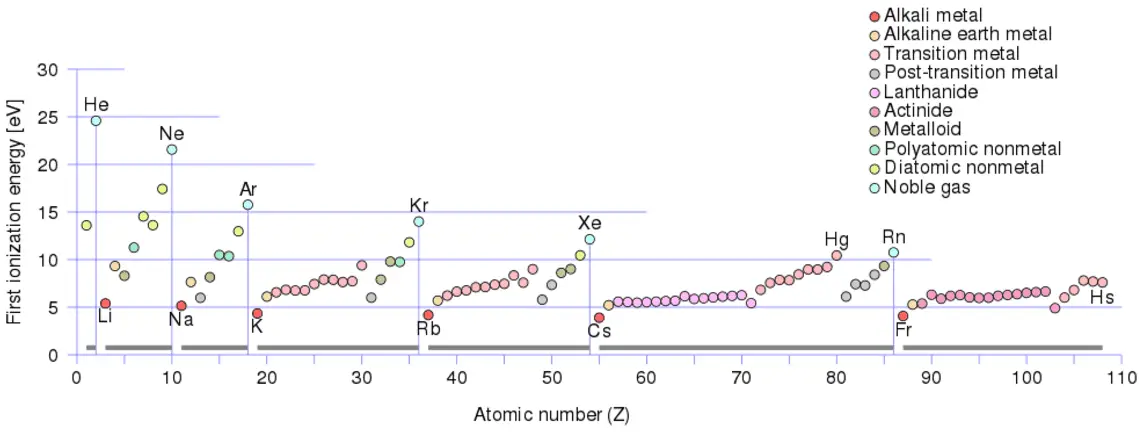
Im Allgemeinen nimmt die Ionisierungsenergie zu, wenn eine Gruppe nach oben und über einen Zeitraum von links nach rechts bewegt wird. Außerdem:
- Die Ionisierungsenergie ist für die Alkalimetalle am niedrigsten, die ein einzelnes Elektron außerhalb einer geschlossenen Hülle haben.
- Die Ionisierungsenergie steigt über eine Reihe auf das periodische Maximum für die Edelgase, die geschlossene Schalen haben
Zum Beispiel benötigt Natrium nur 496 kJ / mol oder 5,14 eV / Atom, um es zu ionisieren. Andererseits benötigt Neon, das im Periodensystem unmittelbar davor stehende Edelgas, 2081 kJ / mol oder 21,56 eV / Atom.
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: [email protected] oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.
