
Le rayonnement ionisant est tout rayonnement ( particules ou ondes électromagnétiques ) qui transporte suffisamment d’énergie pour éliminer les électrons des atomes ou des molécules, les ionisant ainsi. Pour les rayonnements ionisants, l’énergie cinétique des particules ( photons, électrons, etc. ) est suffisante et la particule peut ioniser (pour former des ions en perdant des électrons) des atomes cibles pour former des ions.
La frontière entre les rayonnements ionisants et non ionisants n’est pas clairement définie, car différentes molécules et atomes s’ionisent à différentes énergies. Ceci est typique des ondes électromagnétiques. Parmi les ondes électromagnétiques appartiennent, par ordre croissant de fréquence (énergie) et de longueur d’onde décroissante: les ondes radio, les micro-ondes, le rayonnement infrarouge, la lumière visible, le rayonnement ultraviolet, les rayons X et les rayons gamma. Les rayons gamma , les rayons X , et la partie ultraviolette du spectre plus élevée sont ionisants, alors que l’ultraviolet inférieur, la lumière visible (y compris la lumière laser), infrarouge, micro – ondes et les ondes radio sont considérés comme des rayonnements non ionisants.
Tous les effets des dommages biologiques commencent par la conséquence des interactions de rayonnement avec les atomes formant les cellules. Tous les êtres vivants sont composés d’une ou plusieurs cellules. Chaque partie de votre corps est constituée de cellules ou a été construite par elles. Bien que nous ayons tendance à penser aux effets biologiques en termes d’effet du rayonnement sur les cellules vivantes, en réalité, le rayonnement ionisant , par définition, n’interagit qu’avec les atomes par un processus appelé ionisation.
Le danger des rayonnements ionisants réside dans le fait que les rayonnements sont invisibles et non directement détectables par les sens humains. Les gens ne peuvent ni voir ni ressentir le rayonnement, mais il dépose de l’énergie dans les molécules du corps. L’énergie est transférée en petites quantités pour chaque interaction entre le rayonnement et une molécule et il existe généralement de nombreuses interactions de ce type.
Formes de rayonnement ionisant
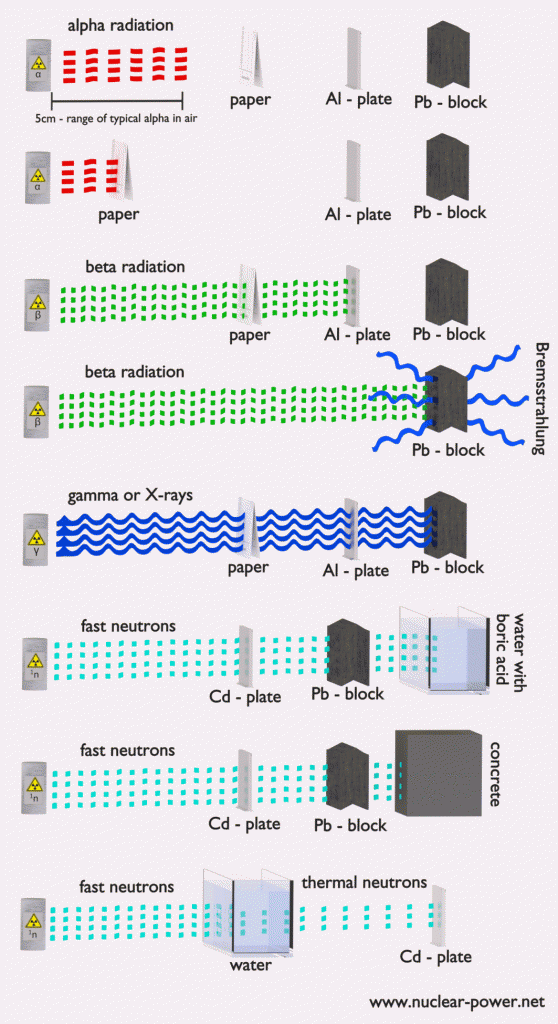 Les rayonnements ionisants sont classés selon la nature des particules ou des ondes électromagnétiques qui créent l’effet ionisant. Ces particules / ondes ont des mécanismes d’ionisation différents et peuvent être regroupées comme:
Les rayonnements ionisants sont classés selon la nature des particules ou des ondes électromagnétiques qui créent l’effet ionisant. Ces particules / ondes ont des mécanismes d’ionisation différents et peuvent être regroupées comme:
- Directement ionisant . Les particules chargées ( noyaux atomiques, électrons, positrons, protons, muons, etc. ) peuvent ioniser les atomes directement par interaction fondamentale à travers la force de Coulomb si elle transporte suffisamment d’énergie cinétique. Ces particules doivent se déplacer à des vitesses relativistes pour atteindre l’énergie cinétique requise. Même les photons (rayons gamma et rayons X) peuvent ioniser les atomes directement (bien qu’ils soient électriquement neutres) grâce à l’effet photoélectrique et à l’effet Compton, mais l’ionisation secondaire (indirecte) est beaucoup plus importante.
- Rayonnement alpha . Le rayonnement alpha se compose de particules alpha à haute énergie / vitesse. La production de particules alpha est appelée désintégration alpha. Les particules alpha se composent de deux protons et de deux neutrons liés ensemble en une particule identique à un noyau d’hélium. Les particules alpha sont relativement grandes et portent une double charge positive. Ils ne sont pas très pénétrants et un morceau de papier peut les arrêter. Ils ne parcourent que quelques centimètres mais déposent toutes leurs énergies le long de leurs courts trajets.
- Rayonnement bêta . Le rayonnement bêta se compose d’électrons libres ou de positrons à des vitesses relativistes. Les particules bêta (électrons) sont beaucoup plus petites que les particules alpha. Ils portent une seule charge négative. Ils sont plus pénétrants que les particules alpha, mais un mince métal d’aluminium peut les arrêter. Ils peuvent parcourir plusieurs mètres mais déposent moins d’énergie à n’importe quel point de leur trajet que les particules alpha.
- Ionisant indirectement . Les rayonnements ionisants indirects sont des particules électriquement neutres et n’interagissent donc pas fortement avec la matière. La majeure partie des effets d’ionisation sont dus aux ionisations secondaires.
- Rayonnement photonique ( rayons gamma ou rayons X). Le rayonnement photonique est constitué de photons de haute énergie . Ces photons sont des particules / ondes (dualité onde-particule) sans masse au repos ni charge électrique. Ils peuvent parcourir 10 mètres ou plus dans les airs. Il s’agit d’une longue distance par rapport aux particules alpha ou bêta. Cependant, les rayons gamma déposent moins d’énergie le long de leurs trajectoires. Le plomb, l’eau et le béton arrêtent le rayonnement gamma. Les photons (rayons gamma et rayons X) peuvent ioniser les atomes directement par l’effet photoélectrique et l’effet Compton, où l’électron relativement énergétique est produit. L’électron secondaire continuera à produire de multiples événements d’ ionisation , donc l’ionisation secondaire (indirecte) est beaucoup plus importante.
- Rayonnement neutronique . Le rayonnement neutronique se compose de neutrons libres à toutes les énergies / vitesses. Les neutrons peuvent être émis par fission nucléaire ou par désintégration de certains atomes radioactifs. Les neutrons ont une charge électrique nulle et ne peuvent pas provoquer directement l’ionisation. Les neutrons n’ionisent la matière qu’indirectement . Par exemple, lorsque les neutrons frappent les noyaux d’hydrogène, il en résulte un rayonnement protonique (protons rapides). Les neutrons peuvent aller des particules à haute vitesse et haute énergie aux particules à basse vitesse et basse énergie (appelées neutrons thermiques). Les neutrons peuvent parcourir des centaines de mètres dans l’air sans aucune interaction.
Rayonnement à LET élevé et à faible LET
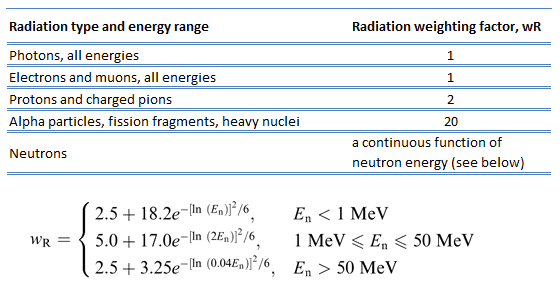
Comme il a été écrit, chaque type de rayonnement interagit avec la matière d’une manière différente . Par exemple, des particules chargées de hautes énergies peuvent directement ioniser les atomes. Les particules alpha sont assez massives et portent une double charge positive, elles ont donc tendance à parcourir seulement une courte distance et à ne pas pénétrer très loin dans les tissus, voire pas du tout. Cependant, les particules alpha déposeront leur énergie sur un plus petit volume (éventuellement seulement quelques cellules si elles pénètrent dans un corps) et causeront plus de dommages à ces quelques cellules.
Les particules bêta (électrons) sont beaucoup plus petites que les particules alpha. Ils portent une seule charge négative. Ils sont plus pénétrants que les particules alpha. Ils peuvent parcourir plusieurs mètres mais déposent moins d’énergie à n’importe quel point de leur trajet que les particules alpha. Cela signifie que les particules bêta ont tendance à endommager plus de cellules, mais avec moins de dommages à chacune. D’autre part, les particules électriquement neutres n’interagissent qu’indirectement, mais peuvent également transférer une partie ou la totalité de leurs énergies à la matière.
Cela simplifierait certainement les choses si les effets biologiques des rayonnements étaient directement proportionnels à la dose absorbée . Malheureusement, les effets biologiques dépendent également de la façon dont la dose absorbée est distribuée le long du trajet du rayonnement. Des études ont montré que le rayonnement alpha et neutronique cause des dommages biologiques plus importants pour un dépôt d’énergie donné par kg de tissu que le rayonnement gamma. Il a été découvert que les effets biologiques de tout rayonnement augmentent avec le transfert d’énergie linéaire (LET). En bref, les dommages biologiques causés par les rayonnements à haut LET ( particules alpha , protons ou neutrons)) est bien supérieure à celle des rayonnements à faible LET ( rayons gamma ). En effet, les tissus vivants peuvent plus facilement réparer les dommages causés par les rayonnements qui sont répartis sur une grande surface que ceux qui sont concentrés sur une petite zone. Bien sûr, à des niveaux d’exposition très élevés, les rayons gamma peuvent encore causer beaucoup de dommages aux tissus.
Parce que plus de dommages biologiques sont causés pour la même dose physique (c.-à-d. La même énergie déposée par unité de masse de tissu), un gris de rayonnement alpha ou neutronique est plus nocif qu’un gray de rayonnement gamma. Ce fait que les rayonnements de différents types (et énergies) donnent des effets biologiques différents pour la même dose absorbée est décrit en termes de facteurs connus sous le nom d’ efficacité biologique relative (EBR) et de facteur de pondération des rayonnements (wR).
Le facteur de pondération du rayonnement est un facteur sans dimension utilisé pour déterminer la dose équivalente à partir de la dose absorbée moyenne sur un tissu ou un organe et est basé sur le type de rayonnement absorbé. La dose pondérée résultante a été désignée comme la dose équivalente d’organe ou de tissu:
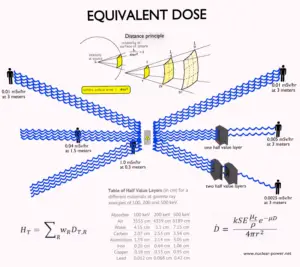 Une dose équivalente d’ un Sievert représente la quantité de dose de rayonnement qui est équivalente, en termes de dommages biologiques spécifiés , à un gris de rayons X ou de rayons gamma . La dose équivalente est une quantité non physique (w R est dérivée des conséquences biologiques des rayonnements ionisants) largement utilisée en dosimétrie mesurée par des dosimètres. La dose équivalente est désignée par la CIPR comme une «quantité limite»; spécifier des limites d’exposition pour garantir que «la survenue d’effets stochastiques sur la santé soit maintenue en dessous de niveaux inacceptables et que les réactions tissulaires soient évitées».
Une dose équivalente d’ un Sievert représente la quantité de dose de rayonnement qui est équivalente, en termes de dommages biologiques spécifiés , à un gris de rayons X ou de rayons gamma . La dose équivalente est une quantité non physique (w R est dérivée des conséquences biologiques des rayonnements ionisants) largement utilisée en dosimétrie mesurée par des dosimètres. La dose équivalente est désignée par la CIPR comme une «quantité limite»; spécifier des limites d’exposition pour garantir que «la survenue d’effets stochastiques sur la santé soit maintenue en dessous de niveaux inacceptables et que les réactions tissulaires soient évitées».
Énergie d’ionisation
L’énergie d’ionisation , également appelée potentiel d’ionisation , est l’énergie nécessaire pour retirer un électron de l’atome neutre.
Énergie X + → X + + e –
où X est n’importe quel atome ou molécule capable d’être ionisé, X + est cet atome ou molécule avec un électron retiré (ion positif), et e – est l’électron retiré.
Un atome d’azote, par exemple, nécessite l’énergie d’ionisation suivante pour éliminer l’électron le plus à l’extérieur.
N + IE → N + + e – IE = 14,5 eV
L’énergie d’ionisation associée à l’élimination du premier électron est la plus couramment utilisée. La n e énergie d’ionisation se réfère à la quantité d’énergie nécessaire pour retirer un électron de l’espèce avec une charge de ( n -1).
1ère énergie d’ionisation
X → X + + e –
2ème énergie d’ionisation
X + → X 2+ + e –
3e énergie d’ionisation
X 2+ → X 3+ + e –
Énergie d’ionisation pour différents éléments
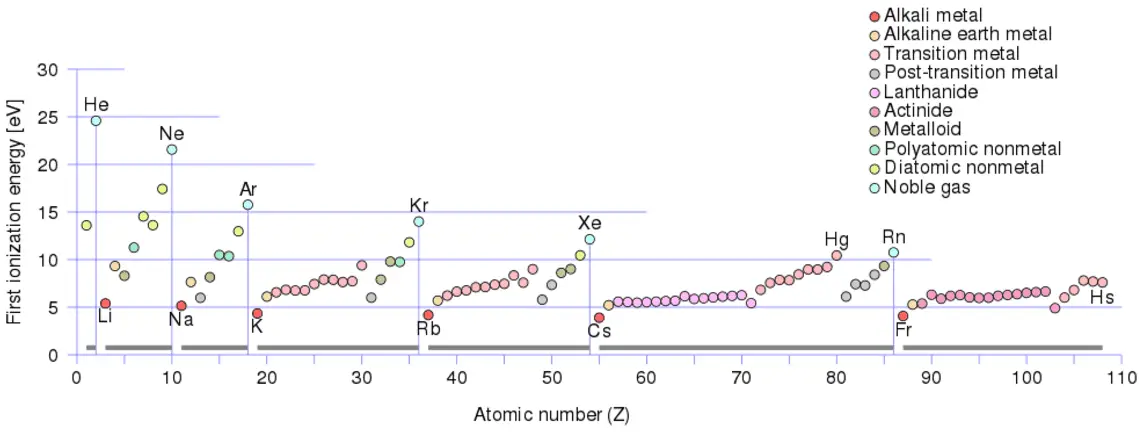
Il existe une énergie d’ionisation pour chaque électron successif retiré. Les électrons qui entourent le noyau se déplacent sur des orbites assez bien définies. Certains de ces électrons sont plus étroitement liés dans l’atome que d’autres. Par exemple, seulement 7,38 eV sont nécessaires pour retirer l’électron le plus à l’extérieur d’un atome de plomb, tandis que 88 000 eV sont requis pour éliminer l’électron le plus à l’intérieur. Aide à comprendre la réactivité des éléments (en particulier les métaux, qui perdent des électrons).
En général, l’énergie d’ionisation augmente en remontant un groupe et en se déplaçant de gauche à droite sur une période. De plus:
- L’énergie d’ionisation est la plus faible pour les métaux alcalins qui ont un seul électron à l’extérieur d’une coquille fermée.
- L’énergie d’ionisation augmente à travers une rangée sur le maximum périodique pour les gaz nobles qui ont des coquilles fermées
Par exemple, le sodium ne nécessite que 496 kJ / mol ou 5,14 eV / atome pour l’ioniser. Par contre le néon, le gaz noble, qui le précède immédiatement dans le tableau périodique, nécessite 2081 kJ / mol ou 21,56 eV / atome.
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: [email protected] ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci
