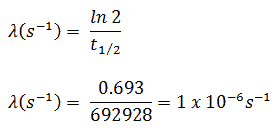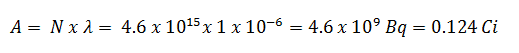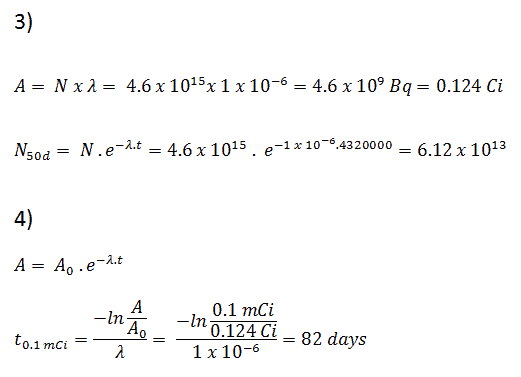Lei de Decaimento – Equação – Fórmula
A lei de decaimento radioativo afirma que a probabilidade por unidade de tempo que um núcleo decairá é uma constante, independente do tempo. Essa constante é chamada constante de decaimento e é denotada por λ, “lambda”. Essa probabilidade constante pode variar muito entre os diferentes tipos de núcleos, levando a muitas taxas diferentes de decaimento observadas. O decaimento radioativo de certo número de átomos (massa) é exponencial no tempo.
Lei de decaimento radioativo: N = Ne- λt
A taxa de decaimento nuclear também é medida em termos de meia-vida . A meia-vida é a quantidade de tempo que um determinado isótopo leva para perder metade de sua radioatividade. Se um radioisótopo tiver meia-vida de 14 dias, metade de seus átomos terá decaimento em 14 dias. Em mais 14 dias, metade da metade restante decairá e assim por diante. As meias-vidas variam de milionésimos de segundo para produtos de fissão altamente radioativos a bilhões de anos para materiais de longa duração (como o urânio que ocorre naturalmente). Notar quemeia-vida curta acompanha grandes constantes de decaimento. O material radioativo com meia-vida curta é muito mais radioativo (no momento da produção), mas obviamente perderá sua radioatividade rapidamente. Não importa quanto tempo a meia-vida seja curta ou curta, depois que sete meias-vidas tiverem passado, resta menos de 1% da atividade inicial.
A lei de decaimento radioativo também pode ser derivada para cálculos de atividade ou massa de cálculos de material radioativo:
(Número de núcleos) N = Ne -λt (Atividade) A = Ae -λt (Massa) m = me -λt
, onde N (número de partículas) é o número total de partículas na amostra, A (atividade total) é o número de decaimentos por unidade de tempo de uma amostra radioativa, m é a massa do material radioativo restante.
Decaimento constante e meia-vida – Equação – Fórmula
Nos cálculos de radioatividade, um dos dois parâmetros ( constante de decaimento ou meia-vida ), que caracterizam a taxa de decaimento, deve ser conhecido. Existe uma relação entre a meia-vida (t 1/2 ) e a constante de decaimento λ. O relacionamento pode ser derivado da lei de decaimento, definindo N = ½ N o . Isto dá:
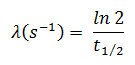 onde ln 2 (o logaritmo natural de 2) é igual a 0,693. Se a constante de decaimento (λ) for dada, é fácil calcular a meia-vida e vice-versa.
onde ln 2 (o logaritmo natural de 2) é igual a 0,693. Se a constante de decaimento (λ) for dada, é fácil calcular a meia-vida e vice-versa.
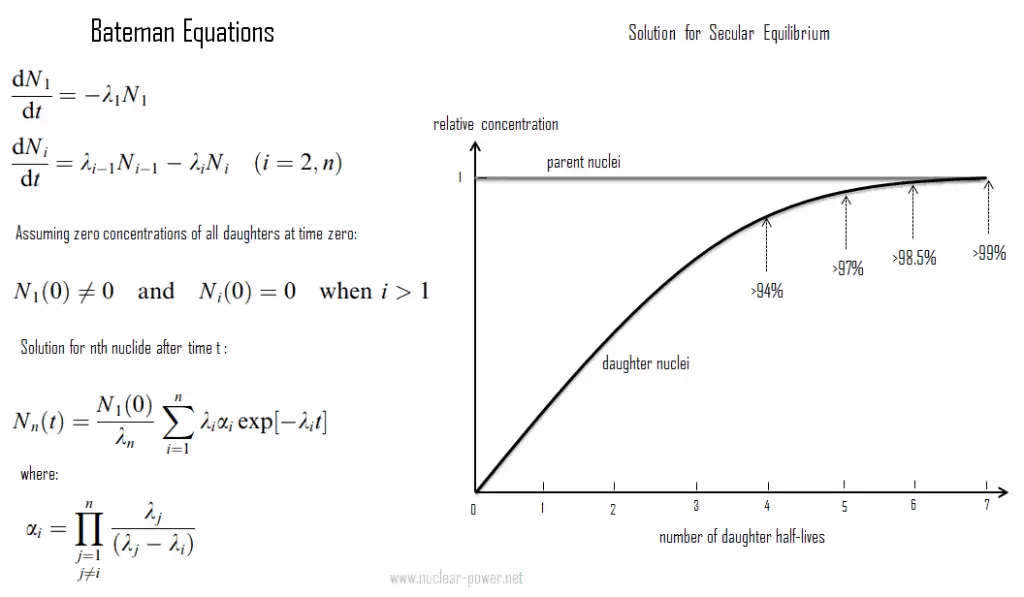
Equações de Bateman
Na física, as equações de Bateman são um conjunto de equações diferenciais de primeira ordem, que descrevem a evolução no tempo das concentrações de nuclídeos em cadeia de decaimento serial ou linear. O modelo foi formulado por Ernest Rutherford em 1905 e a solução analítica para o caso de decaimento radioativo em uma cadeia linear foi fornecida por Harry Bateman em 1910. Esse modelo também pode ser usado em códigos de depleção nuclear para resolver problemas de transmutação e decaimento nuclear.
Por exemplo, o ORIGEN é um sistema de código de computador para calcular o acúmulo, deterioração e processamento de materiais radioativos. O ORIGEN usa um método exponencial de matriz para resolver um grande sistema de equações diferenciais ordinárias lineares de primeira ordem acopladas (semelhantes às equações de Bateman ) com coeficientes constantes.
As equações de Bateman para o caso de decaimento radioativo da série n – nuclídeo em cadeia linear que descreve as concentrações de nuclídeo são as seguintes:
Exemplo – Lei de Decaimento Radioativo
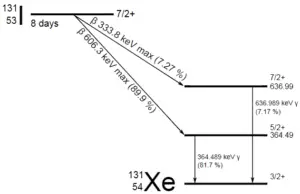 Uma amostra de material contém 1 micrograma de iodo-131. Observe que o iodo-131 desempenha um papel importante como isótopo radioativo presente nos produtos de fissão nuclear e é um dos principais contribuintes para os riscos à saúde quando liberado na atmosfera durante um acidente. O iodo-131 tem uma meia-vida de 8,02 dias.
Uma amostra de material contém 1 micrograma de iodo-131. Observe que o iodo-131 desempenha um papel importante como isótopo radioativo presente nos produtos de fissão nuclear e é um dos principais contribuintes para os riscos à saúde quando liberado na atmosfera durante um acidente. O iodo-131 tem uma meia-vida de 8,02 dias.
Calcular:
- O número de átomos de iodo-131 inicialmente presentes.
- A atividade do iodo-131 nos curies.
- O número de átomos de iodo-131 que permanecerá em 50 dias.
- O tempo necessário para a atividade atingir 0,1 mCi.
Solução:
- O número de átomos de iodo-131 pode ser determinado usando a massa isotópica como abaixo.
N -131 = m I-131 . N A / H I-131
NI -131 = (1 μg) x (6,02 × 10 23 núcleos / mol) / (130,91 g / mol)
NI -131 = 4,6 x 10 15 núcleos
- A atividade do iodo-131 em curies pode ser determinada usando sua constante de decaimento :
O iodo-131 tem meia-vida de 8,02 dias (692928 seg) e, portanto, sua constante de decaimento é:
Usando esse valor para a constante de decaimento, podemos determinar a atividade da amostra:
3) e 4) O número de átomos de iodo-131 que permanecerá em 50 dias (N 50d ) e o tempo necessário para a atividade atingir 0,1 mCi podem ser calculados usando a lei de decaimento:
Como pode ser visto, após 50 dias o número de átomos de iodo-131 e, portanto, a atividade será cerca de 75 vezes menor. Após 82 dias, a atividade será aproximadamente 1200 vezes menor. Portanto, o tempo de dez meias-vidas (fator 2 10 = 1024) é amplamente utilizado para definir a atividade residual.
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: [email protected] ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.