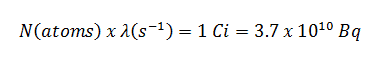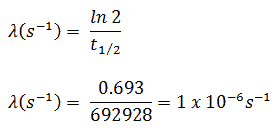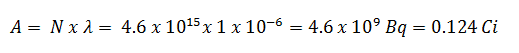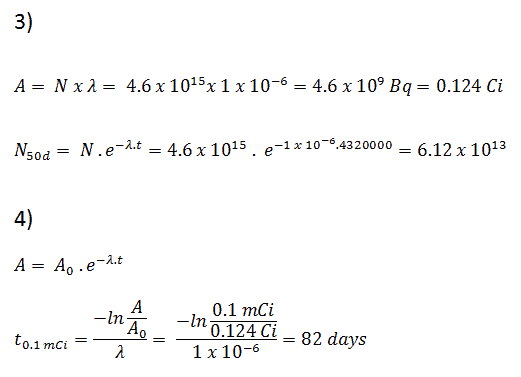En physique nucléaire et en chimie nucléaire, les différentes espèces d’atomes dont les noyaux contiennent un nombre particulier de protons et de neutrons sont appelées nucléides . Les nucléides sont également caractérisés par leurs états d’énergie nucléaire (par exemple nucléide métastable 242m Am). Chaque nucléide est désigné par le symbole chimique de l’élément (cela spécifie Z) avec le numéro de masse atomique en exposant. Les isotopes sont des nucléides qui ont le même numéro atomique et sont donc le même élément, mais diffèrent par le nombre de neutrons.
Il existe des nucléides instables et radioactifs. Ces nucléides sont appelés radionucléides (nucléides radioactifs) ou radioisotopes (isotopes radioactifs). Ces isotopes instables se désintègrent par diverses voies de désintégration radioactive, le plus souvent la désintégration alpha, la désintégration bêta, la désintégration gamma ou la capture d’électrons. De nombreux autres types rares de désintégration, comme la fission spontanée ou l’émission de neutrons, sont connus.
Comme cela a été écrit, la désintégration radioactive des radionucléides est un processus aléatoire au niveau des atomes uniques, en ce sens que, selon la théorie quantique, il est impossible de prédire quand un atome particulier va se désintégrer. En d’autres termes, un noyau d’un radionucléide n’a pas de «mémoire». Un noyau ne «vieillit» pas avec le temps. Ainsi, la probabilité de sa décomposition n’augmente pas avec le temps, mais reste constante quelle que soit la durée d’existence du noyau.
Par conséquent, le taux de décroissance nucléaire peut également être mesuré en termes de demi-vies . Chaque radionucléide a sa propre demi-vie particulière qui ne change jamais, quelle que soit la quantité ou la forme du matériau (c.-à-d. Solide, liquide, gaz, élément ou composé) ou son histoire passée. Si un radio-isotope a une demi-vie de 14 jours, la moitié de ses atomes se seront désintégrés en 14 jours. Dans 14 jours de plus, la moitié de la moitié restante se décomposera, etc.
Les demi-vies varient de millionièmes de seconde pour les produits de fission hautement radioactifs à des milliards d’années pour les matériaux à vie longue (comme l’uranium naturel). Après que cinq demi-vies se soient écoulées, il ne reste que 1/32, ou 3,1%, du nombre original d’atomes. Après sept demi-vies, il ne reste que 1/128, soit 0,78%, des atomes. Le nombre d’atomes existant après 5 à 7 demi-vies peut généralement être considéré comme négligeable.
La fraction de l’activité d’origine restante après les demi-vies suivantes est:
Activité après 1 demi-vie = ½ de l’original
Activité après 2 demi-vies = ½ x ½ = ¼ de l’original
Activité après 3 demi-vies = ½ x ½ x ½ = (½) 3 = 1/8 de l’original
Activité après 4 demi-vies = (½) 4 = 1/16 de l’original
Activité après 5 demi-vies = (½) 5 = 1/32 de l’original
Activité après 6 demi-vies = (½) 6 = 1/64 de l’original
Activité après 7 demi-vies = (½) 7 = 1/128 de l’original
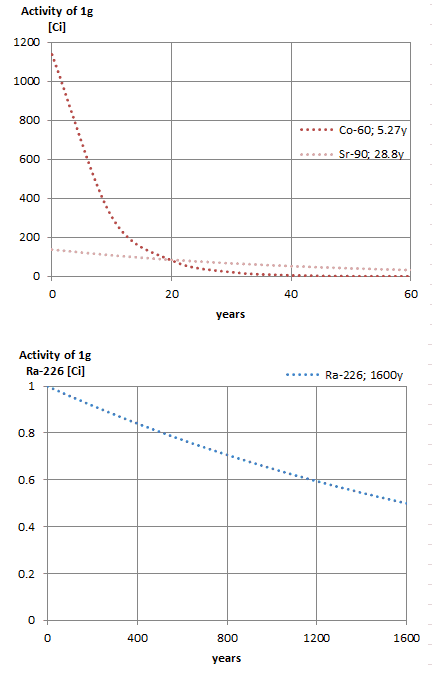 Notez que les courtes demi-vies s’accompagnent de grandes constantes de désintégration. Les matières radioactives à demi-vie courte sont beaucoup plus radioactives (au moment de la production) mais perdront évidemment rapidement leur radioactivité. Quelle que soit la durée ou la durée de la demi-vie, après sept demi-vies, il reste moins de 1% de l’activité initiale.
Notez que les courtes demi-vies s’accompagnent de grandes constantes de désintégration. Les matières radioactives à demi-vie courte sont beaucoup plus radioactives (au moment de la production) mais perdront évidemment rapidement leur radioactivité. Quelle que soit la durée ou la durée de la demi-vie, après sept demi-vies, il reste moins de 1% de l’activité initiale.
La loi de désintégration radioactive stipule que la probabilité par unité de temps qu’un noyau se désintègre est une constante, indépendante du temps. Cette constante est appelée constante de désintégration et est notée λ, « lambda ». Cette probabilité constante peut varier considérablement entre les différents types de noyaux, conduisant aux nombreux taux de désintégration observés différents. La désintégration radioactive d’un certain nombre d’atomes (masse) est exponentielle dans le temps.
Loi de désintégration radioactive: N = Ne -λt
La loi de désintégration radioactive peut également être dérivée pour les calculs d’activité ou les calculs de masse de matières radioactives:
(Nombre de noyaux) N = Ne -λt (Activité) A = Ae -λt (Masse) m = me -λt
, où N (nombre de particules) est le nombre total de particules dans l’échantillon, A (activité totale) est le nombre de désintégrations par unité de temps d’un échantillon radioactif, m est la masse de matière radioactive restante.
Demi-vie et radioactivité des radionucléides
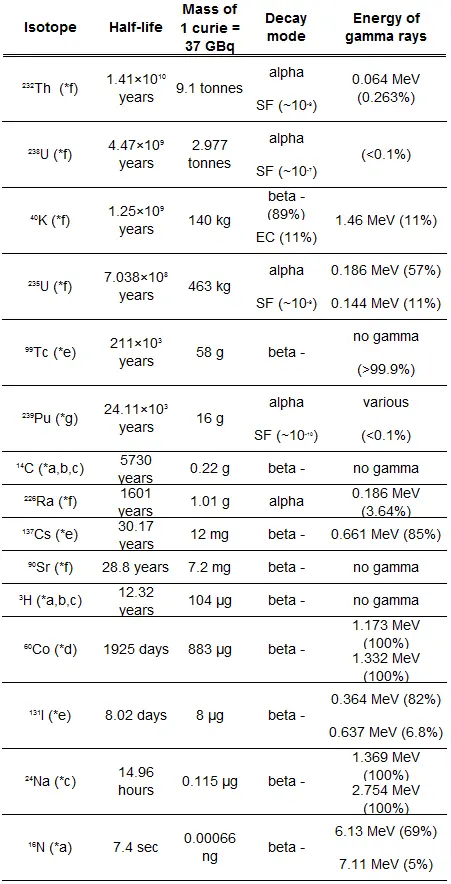
La relation entre la demi-vie et la quantité de radionucléide nécessaire pour donner une activité d’un curie est illustrée sur la figure. Cette quantité de matière peut être calculée en utilisant λ , qui est la constante de désintégration de certains nucléides:
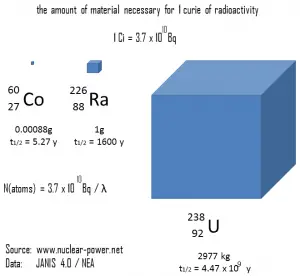 La figure suivante illustre la quantité de matière nécessaire pour 1 curie de radioactivité. Il est évident que plus la demi-vie est longue, plus la quantité de radionucléide nécessaire pour produire la même activité est importante. Bien sûr, la substance à longue durée de vie restera radioactive pendant beaucoup plus longtemps. Comme on peut le voir, la quantité de matière nécessaire pour 1 curie de radioactivité peut varier d’une quantité trop petite pour être vue (0,00088 gramme de cobalt-60), à travers 1 gramme de radium-226, à près de trois tonnes d’ uranium-238 .
La figure suivante illustre la quantité de matière nécessaire pour 1 curie de radioactivité. Il est évident que plus la demi-vie est longue, plus la quantité de radionucléide nécessaire pour produire la même activité est importante. Bien sûr, la substance à longue durée de vie restera radioactive pendant beaucoup plus longtemps. Comme on peut le voir, la quantité de matière nécessaire pour 1 curie de radioactivité peut varier d’une quantité trop petite pour être vue (0,00088 gramme de cobalt-60), à travers 1 gramme de radium-226, à près de trois tonnes d’ uranium-238 .
Exemple – Radioactivité du radionucléide
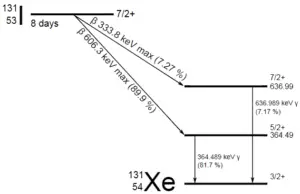 Un échantillon de matériau contient 1 mikrogramme d’iode 131. Il est à noter que l’iode 131 joue un rôle majeur en tant qu’isotope radioactif présent dans les produits de fission nucléaire et qu’il contribue de façon importante aux risques pour la santé lorsqu’il est rejeté dans l’atmosphère lors d’un accident. L’iode 131 a une demi-vie de 8,02 jours.
Un échantillon de matériau contient 1 mikrogramme d’iode 131. Il est à noter que l’iode 131 joue un rôle majeur en tant qu’isotope radioactif présent dans les produits de fission nucléaire et qu’il contribue de façon importante aux risques pour la santé lorsqu’il est rejeté dans l’atmosphère lors d’un accident. L’iode 131 a une demi-vie de 8,02 jours.
Calculer:
- Le nombre d’atomes d’iode-131 initialement présents.
- L’activité de l’iode 131 dans les curies.
- Le nombre d’atomes d’iode 131 qui resteront dans 50 jours.
- Temps nécessaire à l’activité pour atteindre 0,1 mCi.
Solution:
- Le nombre d’atomes d’iode-131 peut être déterminé en utilisant la masse isotopique comme ci-dessous.
N I-131 = m I-131 . N A / M I-131
N I-131 = (1 μg) x (6,02 × 10 23 noyaux / mol) / (130,91 g / mol)
N I-131 = 4,6 x 10 15 noyaux
- L’activité de l’iode 131 dans les curies peut être déterminée en utilisant sa constante de désintégration :
L’iode 131 a une demi-vie de 8,02 jours (692928 s) et donc sa constante de désintégration est:
En utilisant cette valeur pour la constante de désintégration, nous pouvons déterminer l’activité de l’échantillon:
3) et 4) Le nombre d’atomes d’iode-131 qui resteront dans 50 jours (N 50d ) et le temps qu’il faudra pour que l’activité atteigne 0,1 mCi peuvent être calculés en utilisant la loi de décroissance:
Comme on peut le voir, après 50 jours, le nombre d’atomes d’iode 131 et donc l’activité sera environ 75 fois plus faible. Après 82 jours, l’activité sera environ 1200 fois plus faible. Par conséquent, le temps de dix demi-vies (facteur 2 10 = 1024) est largement utilisé pour définir l’activité résiduelle.
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci