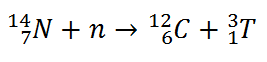Les radionucléides cosmogéniques sont des radionucléides générés par les réactions nucléaires lors de l’interaction entre les rayons cosmiques de haute énergie et les noyaux stables de l’atmosphère. Un des radionucléides cosmogéniques bien connu est le carbone-14, qui est généré par la réaction de 14 N (n, p) 14 C . Les autres isotopes générés sont les suivants: 3 H, 7 Be, 22 Na. La plupart des radionucléides cosmogéniques sont des produits de (n, p), (p, n) et surtout des réactions de spallation. Ces réactions nucléaires sont très rapides et se produisent dans un temps comparable au temps de transit d’une particule incidente à travers le noyau (~ 10 -22s). Le temps d’interaction très court permet une interaction d’un seul nucléon uniquement (dans les cas extrêmes). Ces réactions sont appelées réactions nucléaires directes .
Carbone-14
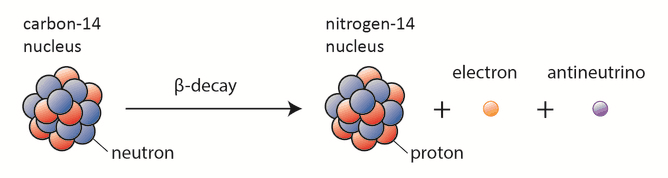
Le seul radionucléide cosmogène à apporter une contribution significative à l’exposition interne de l’homme est le carbone 14. Le carbone 14 radioactif a une demi-vie de 5730 ans et subit une désintégration β− , où le neutron est converti en proton , en électron et en antineutrino électronique :
Malgré cette courte demi-vie par rapport à l’âge de la terre, le carbone 14 est un isotope naturel. Sa présence peut s’expliquer par la simple observation suivante. Notre atmosphère contient de nombreux gaz, dont l’azote-14. De plus, l’atmosphère est constamment bombardée de rayons cosmiques de haute énergie , constitués de protons, de noyaux plus lourds ou de rayons gamma. Ces rayons cosmiques interagissent avec les noyaux de l’atmosphère et produisent également des neutrons de haute énergie . Ces neutrons produits lors de ces collisions peuvent être absorbés par l’azote-14 pour produire un isotope du carbone-14:
Le carbone 14 peut également être produit dans l’atmosphère par d’autres réactions neutroniques, notamment le 13C (n, γ) 14C et le 17O (n, α) 14C. En conséquence, le carbone 14 est formé en continu dans la haute atmosphère par l’interaction des rayons cosmiques avec l’azote atmosphérique. En moyenne, seulement un atome de carbone sur 1,3 x 10 12 dans l’atmosphère est un atome de carbone 14 radioactif. En conséquence, toutes les substances biologiques vivantes contiennent la même quantité de C-14 par gramme de carbone, soit 0,3 Bq d’activité de carbone-14 par gramme de carbone. Le carbone 14 est présent dans le corps humain (13 kg de carbone chez 70 kg d’humain) à un niveau d’environ 3700 Bq (0,1 μCi) avec une demi-vie biologique de 40 jours. Notez que la demi-vie biologiqueest le temps mis pour que la quantité d’un élément particulier dans le corps diminue jusqu’à la moitié de sa valeur initiale en raison de l’élimination par les seuls processus biologiques. Cependant, un atome de carbone se trouve dans les informations génétiques d’environ la moitié des cellules, tandis que le potassium n’est pas un composant de l’ADN. La désintégration d’un atome de carbone 14 à l’intérieur de l’ADN chez une personne se produit environ 50 fois par seconde, transformant un atome de carbone en azote.
La dose annuelle de carbone 14 est estimée à environ 12 μSv / an .
Tant que le système biologique est vivant, le niveau est constant en raison de l’apport constant de tous les isotopes de carbone. Lorsque le système biologique meurt, il arrête d’échanger du carbone avec son environnement, et à partir de là, la quantité de carbone 14 qu’il contient commence à diminuer à mesure que le carbone 14 subit une décroissance radioactive.
Voir aussi: Rencontres Carbon-14
Tritium
Le tritium est le seul radio – isotope naturel de l’hydrogène. Son numéro atomique est naturellement 1 ce qui signifie qu’il y a 1 proton et 1 électron dans la structure atomique. Contrairement au noyau d’hydrogène et au noyau de deutérium, le tritium a 2 neutrons dans le noyau. Le tritium est d’origine naturelle, mais il est extrêmement rare .
Le tritium est produit dans l’atmosphère lorsque les rayons cosmiques entrent en collision avec les molécules d’air. Dans la réaction la plus importante pour la production naturelle, un neutron rapide (qui doit avoir une énergie supérieure à 4,0 MeV) interagit avec l’azote atmosphérique:
Dans le monde, la production de tritium d’origine naturelle est de 148 pétabecquerels par an. En conséquence, l’eau tritiée produite participe au cycle de l’eau.
- environ 400 Bq / m 3 dans l’eau continentale
- environ 100 Bq / m 3 dans les océans
Le tritium est un isotope radioactif, mais il émet une forme de rayonnement très faible, une particule bêta de faible énergie semblable à un électron. Il s’agit d’un émetteur bêta pur (c’est-à-dire un émetteur bêta sans rayonnement gamma d’ accompagnement ). L’énergie cinétique de l’électron varie, avec une moyenne de 5,7 keV, tandis que l’énergie restante est emportée par l’ antineutrino électronique presque indétectable . Une si faible énergie d’électrons provoque, que l’électron ne peut pas pénétrer la peau ou même ne voyage pas très loin dans l’air. Les particules bêta du tritium ne peuvent pénétrer que dans environ 6,0 mm d’air. Le tritium se désintègre via une désintégration bêta négative en hélium-3 avec une demi-vie de 12,3 ans .
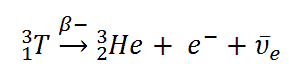 Par conséquent, le tritium présente un risque pour la santé en raison de l’exposition interne uniquement après ingestion dans l’eau potable ou les aliments, ou par inhalation ou absorption par la peau. Le tritium absorbé par l’organisme est uniformément réparti entre tous les tissus mous. Une dose annuelle moyenne provenant de l’apport naturel de tritium est de 0,01 μSv .
Par conséquent, le tritium présente un risque pour la santé en raison de l’exposition interne uniquement après ingestion dans l’eau potable ou les aliments, ou par inhalation ou absorption par la peau. Le tritium absorbé par l’organisme est uniformément réparti entre tous les tissus mous. Une dose annuelle moyenne provenant de l’apport naturel de tritium est de 0,01 μSv .
En cas d’ingestion ou d’inhalation artificielle de tritium, une mi-temps biologique de tritium est de 10 jours pour HTO et de 40 jours pour OBT (tritium lié organiquement) formé à partir de HTO dans le corps des adultes. Il a également été démontré que la mi-temps biologique de l’HTO dépend fortement de nombreuses variables et varie d’environ 4 à 18 jours. Pendant les mois les plus chauds, la demi-vie moyenne est inférieure, ce qui est attribué à l’augmentation de l’apport en eau. De plus, boire de plus grandes quantités d’alcool réduira la demi-vie biologique de l’eau dans le corps.
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci