La biologie des rayonnements (également connue sous le nom de radiobiologie ) est une science médicale qui implique l’étude des effets biologiques des rayonnements ionisants sur les tissus vivants. Le rayonnement est tout autour de nous. Dans, autour et au-dessus du monde dans lequel nous vivons. C’est une force d’énergie naturelle qui nous entoure. C’est une partie de notre monde naturel qui est là depuis la naissance de notre planète. Que la source de rayonnement soit naturelle ou artificielle, que ce soit une forte dose de rayonnement ou une petite dose, il y aura des effets biologiques. En général, les rayonnements ionisants sont nocifs et potentiellement mortels pour les êtres vivants, mais peuvent avoir des avantages pour la santé en médecine, par exemple en radiothérapie pour le traitement du cancer et de la thyréotoxicose. Ce chapitre résume brièvement les conséquences à court et à long terme qui peuvent résulter d’une exposition aux rayonnements.
Dommages cellulaires – Radiobiologie
Tous les effets des dommages biologiques commencent par la conséquence des interactions de rayonnement avec les atomes formant les cellules. Tous les êtres vivants sont composés d’une ou plusieurs cellules. Chaque partie de votre corps est constituée de cellules ou a été construite par elles. Bien que nous ayons tendance à penser aux effets biologiques en termes d’effet du rayonnement sur les cellules vivantes, en réalité, le rayonnement ionisant , par définition, n’interagit qu’avec les atomes par un processus appelé ionisation. Pour le rayonnement ionisant, l’énergie cinétique des particules ( photons, électrons, etc. ) du rayonnement ionisant est suffisante et la particule peut ioniser (pour former des ions en perdant des électrons) des atomes cibles pour former des ions. Un simple rayonnement ionisant peut faire tomber des électrons d’un atome.
Il existe deux mécanismes par lesquels le rayonnement affecte finalement les cellules. Ces deux mécanismes sont communément appelés:
- Effets directs . Les effets directs sont causés par le rayonnement, lorsque le rayonnement interagit directement avec les atomes de la molécule d’ ADN ou un autre composant cellulaire essentiel à la survie de la cellule. La probabilité que le rayonnement interagisse avec la molécule d’ADN est très faible car ces composants critiques constituent une si petite partie de la cellule.
- Effets indirects . Les effets indirects sont causés par l’interaction du rayonnement généralement avec les molécules d’eau . Chaque cellule, comme c’est le cas pour le corps humain, est principalement de l’eau. Les rayonnements ionisants peuvent rompre les liaisons qui maintiennent la molécule d’eau ensemble, produisant des radicaux tels que l’hydroxyle OH, l’anion superoxyde O 2 – et d’autres. Ces radicaux peuvent contribuer à la destruction de la cellule.
Un grand nombre de cellules de tout type particulier est appelé tissu . Si ce tissu forme une unité fonctionnelle spécialisée, il est appelé un organe. Le type et le nombre de cellules affectées sont également un facteur important. Certaines cellules et certains organes du corps sont plus sensibles aux rayonnements ionisants que d’autres .
La sensibilité de divers types de cellules aux rayonnements ionisants est très élevée pour les tissus constitués de cellules qui se divisent rapidement comme celles que l’on trouve dans la moelle osseuse, l’estomac, les intestins, les organes reproducteurs mâles et femelles et les fœtus en développement. En effet, la division des cellules nécessite des informations ADN correctes pour que la progéniture de la cellule survive. Une interaction directe du rayonnement avec une cellule active pourrait entraîner la mort ou la mutation de la cellule, tandis qu’une interaction directe avec l’ADN d’une cellule dormante aurait moins d’effet.
En conséquence, les cellules vivantes peuvent être classées en fonction de leur taux de reproduction, ce qui indique également leur sensibilité relative aux rayonnements. Par conséquent, les cellules à reproduction active sont plus sensibles aux rayonnements ionisants que les cellules qui composent la peau, les reins ou le foie. Les cellules nerveuses et musculaires sont les plus lentes à se régénérer et sont les cellules les moins sensibles.
 La sensibilité des différents organes du corps humain est en corrélation avec la sensibilité relative des cellules dont ils sont composés. Dans la pratique, cette sensibilité est représentée par le facteur de pondération tissulaire , w T , qui est le facteur par lequel la dose équivalente dans un tissu ou un organe T est pondérée pour représenter la contribution relative de ce tissu ou de cet organe au préjudice total pour la santé résultant de irradiation uniforme du corps (ICRP 1991b).
La sensibilité des différents organes du corps humain est en corrélation avec la sensibilité relative des cellules dont ils sont composés. Dans la pratique, cette sensibilité est représentée par le facteur de pondération tissulaire , w T , qui est le facteur par lequel la dose équivalente dans un tissu ou un organe T est pondérée pour représenter la contribution relative de ce tissu ou de cet organe au préjudice total pour la santé résultant de irradiation uniforme du corps (ICRP 1991b).
Si une personne n’est irradiée que partiellement, la dose dépendra fortement du tissu irradié. Par exemple, une dose gamma de 10 mSv pour tout le corps et une dose de 50 mSv pour la thyroïde sont les mêmes, en termes de risque, qu’une dose pour tout le corps de 10 + 0,04 x 50 = 12 mSv.
Rayonnement à LET élevé et à faible LET
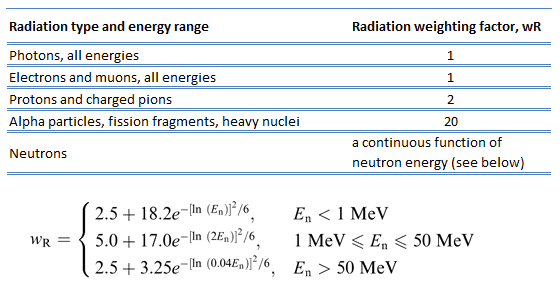
Comme il a été écrit, chaque type de rayonnement interagit avec la matière d’une manière différente . Par exemple, des particules chargées de hautes énergies peuvent directement ioniser les atomes. Les particules alpha sont assez massives et portent une double charge positive, elles ont donc tendance à parcourir seulement une courte distance et à ne pas pénétrer très loin dans les tissus, voire pas du tout. Cependant, les particules alpha déposeront leur énergie sur un plus petit volume (éventuellement seulement quelques cellules si elles pénètrent dans un corps) et causeront plus de dommages à ces quelques cellules.
Les particules bêta (électrons) sont beaucoup plus petites que les particules alpha. Ils portent une seule charge négative. Ils sont plus pénétrants que les particules alpha. Ils peuvent parcourir plusieurs mètres mais déposent moins d’énergie à n’importe quel point de leur trajet que les particules alpha. Cela signifie que les particules bêta ont tendance à endommager plus de cellules, mais avec moins de dommages à chacune. D’autre part, les particules électriquement neutres n’interagissent qu’indirectement, mais peuvent également transférer une partie ou la totalité de leurs énergies à la matière.
Cela simplifierait certainement les choses si les effets biologiques des rayonnements étaient directement proportionnels à la dose absorbée . Malheureusement, les effets biologiques dépendent également de la façon dont la dose absorbée est distribuée le long du trajet du rayonnement. Des études ont montré que le rayonnement alpha et neutronique cause des dommages biologiques plus importants pour un dépôt d’énergie donné par kg de tissu que le rayonnement gamma. Il a été découvert que les effets biologiques de tout rayonnement augmentent avec le transfert d’énergie linéaire (LET). En bref, les dommages biologiques causés par les rayonnements à haut LET ( particules alpha , protons ou neutrons)) est bien supérieure à celle des rayonnements à faible LET ( rayons gamma ). En effet, les tissus vivants peuvent plus facilement réparer les dommages causés par les rayonnements qui sont répartis sur une grande surface que ceux qui sont concentrés sur une petite zone. Bien sûr, à des niveaux d’exposition très élevés, les rayons gamma peuvent encore causer beaucoup de dommages aux tissus.
Parce que plus de dommages biologiques sont causés pour la même dose physique (c.-à-d. La même énergie déposée par unité de masse de tissu), un gris de rayonnement alpha ou neutronique est plus nocif qu’un gray de rayonnement gamma. Ce fait que les rayonnements de différents types (et énergies) donnent des effets biologiques différents pour la même dose absorbée est décrit en termes de facteurs connus sous le nom d’ efficacité biologique relative (EBR) et de facteur de pondération des rayonnements (wR).
Dose aiguë et dose chronique
Les effets biologiques des rayonnements et leurs conséquences dépendent fortement du niveau de débit de dose obtenu. En radiobiologie, le débit de dose est une mesure de l’intensité (ou de la force) de la dose de rayonnement. Des doses faibles sont courantes dans la vie de tous les jours. Dans les points suivants, il existe quelques exemples d’exposition aux rayonnements, qui peuvent être obtenus à partir de diverses sources.
- 05 µSv – Dormir à côté de quelqu’un
- 09 µSv – Vivant à moins de 30 miles d’une centrale nucléaire pendant un an
- 1 µSv – Manger une banane
- 3 µSv – Vivant à moins de 50 miles d’une centrale à charbon pendant un an
- 10 µSv – Dose journalière moyenne reçue du milieu naturel
- 20 µSv – Radiographie thoracique
Du point de vue des conséquences biologiques, il est très important de distinguer les doses reçues sur des périodes courtes et prolongées . Par conséquent, les effets biologiques des rayonnements sont généralement divisés en deux catégories.
- Doses aiguës . Une « dose aiguë » ( dose de haut niveau à court terme) est une dose qui se produit sur une courte période de temps, c’est-à-dire dans la journée.
- Doses chroniques . Une « dose chronique » ( dose faible à long terme) est une dose qui se poursuit pendant une période de temps prolongée, c’est-à-dire des semaines et des mois, de sorte qu’elle est mieux décrite par un débit de dose.
Des doses élevées ont tendance à tuer les cellules, tandis que de faibles doses ont tendance à les endommager ou à les modifier. Des doses élevées peuvent provoquer des brûlures radiales visuellement dramatiques et / ou une mort rapide par syndrome de rayonnement aigu . Il est peu probable que des doses aiguës inférieures à 250 mGy aient des effets observables. Des doses aiguës d’environ 3 à 5 Gy ont 50% de chances de tuer une personne quelques semaines après l’exposition, si une personne ne reçoit aucun traitement médical.
De faibles doses réparties sur de longues périodes ne causent pas de problème immédiat à aucun organe du corps. Les effets de faibles doses de rayonnement se produisent au niveau de la cellule et les résultats peuvent ne pas être observés pendant de nombreuses années. De plus, certaines études démontrent que la plupart des tissus humains présentent une tolérance plus prononcée aux effets des rayonnements à faible LET en cas d’exposition prolongée par rapport à une exposition unique à une dose similaire.
Effets déterministes et stochastiques
En radiobiologie, la plupart des effets néfastes sur la santé de l’exposition aux rayonnements sont généralement divisés en deux grandes catégories:
- Les effets déterministes sont des effets seuils sur la santé, qui sont directement liés à la dose de rayonnement absorbée et la gravité de l’effet augmente à mesure que la dose augmente.
- Les effets stochastiques se produisent par hasard, se produisant généralement sans seuil de dose. La probabilité d’apparition d’effets stochastiques est proportionnelle à la dose mais la sévérité de l’effet est indépendante de la dose reçue.
Effets déterministes
En radiobiologie, les effets déterministes (ou effets non stochastiques sur la santé) sont des effets sur la santé, qui sont directement liés à la dose de rayonnement absorbée et la gravité de l’effet augmente à mesure que la dose augmente. Les effets déterministes ont un seuil en dessous duquel aucun effet clinique détectable ne se produit. Le seuil peut être très bas (de l’ordre de grandeur de 0,1 Gy ou plus) et peut varier d’une personne à l’autre. Pour des doses comprises entre 0,25 Gy et 0,5 Gy, de légères variations sanguines peuvent être détectées par des évaluations médicales et pour des doses comprises entre 0,5 Gy et 1,5 Gy, des changements sanguins seront notés et des symptômes de nausées, de fatigue, de vomissements se produiront.
Une fois le seuil dépassé, la sévérité d’un effet augmente avec la dose. La raison de la présence de cette dose seuil est que les dommages causés par les radiations (dysfonctionnement grave ou décès) d’une population critique de cellules (des doses élevées ont tendance à tuer les cellules) dans un tissu donné doivent être maintenus avant que la blessure ne soit exprimée sous une forme cliniquement pertinente. . Par conséquent, les effets déterministes sont également appelés réaction tissulaire . Ils sont également appelés effets non stochastiques pour contraster avec des effets stochastiques aléatoires (par exemple, induction d’un cancer).
Les effets déterministes ne sont pas nécessairement plus ou moins graves que les effets stochastiques. Des doses élevées peuvent provoquer des brûlures radiales visuellement dramatiques et / ou une mort rapide par syndrome de rayonnement aigu . Il est peu probable que des doses aiguës inférieures à 250 mGy aient des effets observables. Des doses aiguës d’environ 3 à 5 Gy ont 50% de chances de tuer une personne quelques semaines après l’exposition, si une personne ne reçoit aucun traitement médical. Des effets déterministes peuvent à terme conduire à une nuisance temporaire voire à un décès. Exemples d’effets déterministes:
Voici des exemples d’effets déterministes :
- Syndrome de radiation aiguë, par radiation aiguë de tout le corps
- Le rayonnement brûle, du rayonnement à une surface corporelle particulière
- Thyroïdite radio-induite, un effet secondaire potentiel de la radiothérapie contre l’hyperthyroïdie
- Syndrome de radiation chronique, dû à une radiation à long terme.
- Lésion pulmonaire radio-induite, par exemple de la radiothérapie aux poumons
Doses létales de rayonnement
La dose létale de rayonnement (LD) est une indication de la quantité de rayonnement létale. En radioprotection, la dose létale médiane , LD XY, est généralement utilisée. Par exemple, la dose de rayonnement susceptible de provoquer la mort de 50% des personnes irradiées dans les 30 jours est de DL 50/30 . La LD 1 est la dose qui devrait causer la mort de 1% des personnes irradiées, par conséquent, la DL 99 est mortelle pour toutes les personnes (99%) irradiées. Il est également très important de savoir si une personne reçoit ou non des soins médicaux. Plus une dose de rayonnement aiguë est élevée, plus la possibilité qu’elle tue l’individu est grande. Pour un adulte en bonne santé, la DL 50 est estimé entre 3 et 5 Gy.
- 2,5 Sv – Dose qui tue un humain avec un risque de 1% (LD 1 ), si la dose est reçue sur une très courte durée .
- 5 Sv – Dose qui tue un humain avec un risque de 50% dans les 30 jours (DL 50/30 ), si la dose est reçue sur une très courte durée . La cause du décès sera la perte de la fonction de la moelle osseuse.
- 8 Sv – Dose qui tue un humain avec un risque de 99% (DL 99 ), si la dose est reçue sur une très courte durée . Aux alentours de 10 Gy, une inflammation aiguë des poumons peut survenir et entraîner la mort.
Les données de dose létale données ci-dessus s’appliquent aux doses gamma aiguës délivrées en très peu de temps, par exemple quelques minutes. Une dose plus élevée est nécessaire pour produire les effets énumérés ci-dessus, si la dose est reçue sur une période de plusieurs heures ou plus.
Effets stochastiques
En radiobiologie, les effets stochastiques des rayonnements ionisants se produisent par hasard, se produisant généralement sans seuil de dose. La probabilité d’apparition d’ effets stochastiques est proportionnelle à la dose mais la sévérité de l’effet est indépendante de la dose reçue. Les effets biologiques des rayonnements sur les personnes peuvent être regroupés en effets somatiques et héréditaires . Les effets somatiques sont ceux subis par la personne exposée. Les effets héréditaires sont ceux subis par la progéniture de l’individu exposé. Le risque de cancer est généralement mentionné comme le principal effet stochastique des rayonnements ionisants, mais les troubles héréditaires sont également des effets stochastiques.
Selon la CIPR:
(83) Sur la base de ces calculs, la Commission propose des coefficients de probabilité nominaux pour le risque de cancer ajusté au détriment de 5,5 x 10 -2 Sv -1 pour l’ensemble de la population et de 4,1 x 10 -2 Sv -1 pour les travailleurs adultes. Pour les effets héréditaires, le risque nominal ajusté au détriment dans l’ensemble de la population est estimé à 0,2 x 10 -2 Sv -1 et chez les travailleurs adultes à 0,1 x 10 -2 Sv -1 .
Référence spéciale: CIPR, 2007. Les recommandations de 2007 de la Commission internationale de protection radiologique. Publication 103 de la CIPR. Ann. ICRP 37 (2-4).
L’unité SI pour la dose efficace , le sievert , représente l’effet biologique équivalent du dépôt d’un joule d’énergie de rayons gamma dans un kilogramme de tissu humain. En conséquence, un sievert représente 5,5% de chances de développer un cancer. Il convient de noter que la dose efficace n’est pas conçue comme une mesure des effets déterministes sur la santé, c’est-à-dire la gravité des lésions tissulaires aiguës qui se produiront certainement, qui est mesurée par la quantité de dose absorbée.
Il existe trois catégories générales d’ effets stochastiques résultant de l’exposition à de faibles doses de rayonnement. Ceux-ci sont:
- Effets génétiques . L’effet génétique est subi par la progéniture de l’individu exposé. Elle implique la mutation de cellules très spécifiques, à savoir les spermatozoïdes ou les ovules. Le rayonnement est un exemple d’agent mutagène physique. Notez que, il existe également de nombreux agents chimiques ainsi que des agents biologiques (tels que les virus) qui provoquent des mutations. Un fait très important à retenir est que le rayonnement augmente le taux de mutation spontanée, mais ne produit aucune nouvelle mutation.
- Effets somatiques . Les effets somatiques sont ceux subis par la personne exposée . L’impact le plus courant de l’irradiation est l’induction stochastique du cancer avec une période latente de plusieurs années ou décennies après l’exposition. Le cancer étant le principal résultat, il est parfois appelé effet cancérigène. Le rayonnement est un exemple de cancérigène physique, tandis que les cigarettes sont un exemple d’agent chimique causant le cancer. Les virus sont des exemples d’agents cancérigènes biologiques.
- Les effets in utero impliquent la production de malformations dans les embryons en développement. Cependant, il s’agit en fait d’un cas particulier de l’effet somatique, puisque l’embryon / fœtus est celui exposé au rayonnement.
On pense que la plupart des effets somatiques résultant de l’exposition aux rayonnements se produisent de manière stochastique. Le modèle le plus largement accepté postule que l’incidence des cancers dus aux rayonnements ionisants augmente linéairement avec la dose de rayonnement efficace à un taux de 5,5% par sievert . Ce modèle est connu sous le nom de modèle linéaire sans seuil (LNT) . Ce modèle suppose qu’il n’y a pas de seuil et que le risque augmente linéairement avec une dose. Si ce modèle linéaire est correct, le rayonnement de fond naturel est la source de rayonnement la plus dangereuse pour la santé publique en général, suivi de l’imagerie médicale en seconde position. Le LNT n’est pas universellement acceptécertains proposent une relation dose-réponse adaptative où de faibles doses sont protectrices et des doses élevées sont préjudiciables. Il convient de souligner qu’un certain nombre d’organisations ne sont pas d’accord avec l’utilisation du modèle linéaire sans seuil pour estimer le risque d’exposition aux rayonnements environnementaux et professionnels de faible intensité.
Radiobiologie et limites de dose
En radioprotection, des limites de dose sont fixées pour limiter les effets stochastiques à un niveau acceptable et pour empêcher complètement les effets déterministes . Notez que les effets stochastiques sont ceux qui résultent du hasard: plus la dose est élevée, plus l’effet est probable. Les effets déterministes sont ceux qui ont normalement un seuil: au-dessus de cela, la sévérité de l’effet augmente avec la dose. Limites de dosesont une composante fondamentale de la radioprotection, et le dépassement de ces limites est contraire à la réglementation des rayonnements dans la plupart des pays. Notez que les limites de dose décrites dans cet article s’appliquent aux opérations de routine. Ils ne s’appliquent pas à une situation d’urgence lorsque la vie humaine est en danger. Ils ne s’appliquent pas dans les situations d’exposition d’urgence où une personne tente de prévenir une situation catastrophique.
Les limites sont divisées en deux groupes, le public et les travailleurs exposés professionnellement. Selon la CIPR, l’exposition professionnelle fait référence à toute exposition subie par les travailleurs au cours de leur travail, à l’exception des
- expositions exclues et expositions d’activités exonérées impliquant des rayonnements ou des sources exonérées
- toute exposition médicale
- le rayonnement de fond naturel local normal.
Le tableau suivant résume les limites de dose pour les travailleurs exposés professionnellement et pour le public:
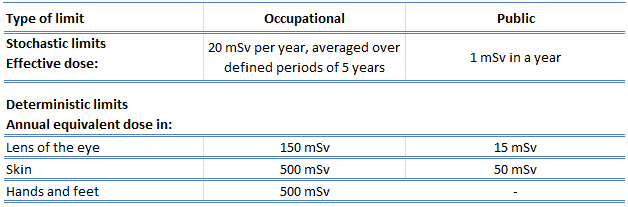
Source de données: CIPR, 2007. Les recommandations de 2007 de la Commission internationale de protection radiologique. Publication 103 de la CIPR. Ann. ICRP 37 (2-4).
Selon la recommandation de la CIPR dans sa déclaration sur les réactions tissulaires du 21 avril 2011, la limite de dose équivalente pour le cristallin de l’exposition professionnelle dans les situations d’exposition planifiée est passée de 150 mSv / an à 20 mSv / an, en moyenne sur des périodes définies de 5 ans, sans dose annuelle sur une seule année supérieure à 50 mSv.
Les limites de dose efficace correspondent à la somme des doses efficaces pertinentes provenant de l’exposition externe au cours de la période spécifiée et de la dose efficace engagée provenant des apports de radionucléides au cours de la même période. Pour les adultes, la dose efficace engagée est calculée pour une période de 50 ans après la prise, tandis que pour les enfants, elle est calculée pour la période allant jusqu’à 70 ans. La limite de dose efficace pour le corps entier de 20 mSv est une valeur moyenne sur cinq ans. La limite réelle est de 100 mSv en 5 ans, avec pas plus de 50 mSv en une année.
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci