Le radon est un gaz noble incolore, inodore et insipide , qui se produit naturellement comme produit de désintégration du radium. Le radon est un élément chimique de numéro atomique 86, ce qui signifie qu’il y a 86 protons et 86 électrons dans la structure atomique. Le symbole chimique du radon est Rn . Tous les isotopes du radon sont radioactifs , mais les deux isotopes du radon radon-222 et radon-220 sont très importants du point de vue de la radioprotection.
-
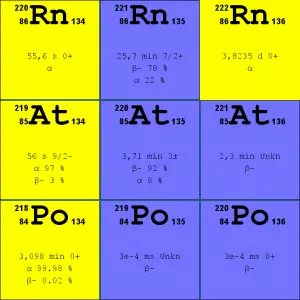
Source: JANIS (Java-based Nuclear Data Information Software); ENDF / B-VII.1 Radon-222 . L’isotope du radon 222 est un produit de désintégration naturel de l’isotope de l’uranium le plus stable (l’uranium 238), il fait donc partie de la série de l’ uranium .
- Radon-220 . L’isotope du radon-220, communément appelé thoron , est un produit de désintégration naturelle de l’isotope du thorium le plus stable ( thorium-232 ), il fait donc partie de la série du thorium .
Il est important de noter que le radon est un gaz noble , alors que tous ses produits de désintégration sont des métaux . Le principal mécanisme d’entrée du radon dans l’atmosphère est la diffusion à travers le sol . En tant que gaz, le radon se diffuse à travers les roches et le sol. Lorsque le radon se désintègre, les isotopes métalliques filles sont des ions qui seront attachés à d’autres molécules comme l’eau et aux particules d’aérosol dans l’air. Par conséquent, toutes les discussions sur les concentrations de radon dans l’environnement se réfèrent au radon-222. Alors que le taux de production moyen de radon-220 (thoron) est à peu près le même que celui du radon-222, la quantité de radon-220 dans l’environnement est bien inférieure à celle du radon-222 en raison d’une demi-vie beaucoup plus courte ( il a moins de temps pour diffuser) du radon-222 (55 secondes, contre 3,8 jours respectivement). Le radon-220 a tout simplement moins de chances de s’échapper du substratum rocheux.
Voir aussi: Radon – Effets sur la santé
Radon – Propriétés
| Élément | Radon |
|---|---|
| Numéro atomique | 86 |
| symbole | Rn |
| Catégorie d’élément | Gaz rare |
| Phase chez STP | Gaz |
| Masse atomique [amu] | 222 |
| Densité à STP [g / cm3] | 9,73 |
| Configuration électronique | [Hg] 6p6 |
| États d’oxydation possibles | 0 |
| Affinité électronique [kJ / mol] | – |
| Électronégativité [échelle de Pauling] | – |
| 1ère énergie d’ionisation [eV] | 10.7485 |
| Année de découverte | 1900 |
| Découvreur | Dorn, Friedrich Ernst |
| Propriétés thermiques | |
| Point de fusion [échelle Celsius] | -71 |
| Point d’ébullition [échelle Celsius] | -61,8 |
| Conductivité thermique [W / m K] | 0,00361 |
| Chaleur spécifique [J / g K] | 0,09 |
| Chaleur de fusion [kJ / mol] | 2,89 |
| Chaleur de vaporisation [kJ / mol] | 16,4 |
Masse atomique du radon
La masse atomique du radon est de 222 u.
Notez que, chaque élément peut contenir plus d’isotopes, donc cette masse atomique résultante est calculée à partir des isotopes naturels et de leur abondance.
L’unité de mesure de la masse est l’ unité de masse atomique (amu) . Une unité de masse atomique équivaut à 1,66 x 10 -24 grammes. Une unité de masse atomique unifiée est approximativement la masse d’un nucléon (soit un seul proton ou neutron) et est numériquement équivalente à 1 g / mol.
Densité de radon
La densité du radon est de 9,73 g / cm 3 .

Densités typiques de diverses substances à pression atmosphérique.
La densité est définie comme la masse par unité de volume . C’est une propriété intensive , qui est mathématiquement définie comme la masse divisée par le volume:
ρ = m / V
En d’autres termes, la densité (ρ) d’une substance est la masse totale (m) de cette substance divisée par le volume total (V) occupé par cette substance. L’unité SI standard est le kilogramme par mètre cube ( kg / m 3 ). L’unité standard anglaise est la masse en livres par pied cube ( lbm / ft 3 ).
Voir aussi: Qu’est-ce que la densité
Voir aussi: Matériaux les plus denses de la Terre
Radon – Point de fusion et point d’ébullition
Point de fusion de radon est -71 ° C .
Point d’ ébullition de radon est -61,8 ° C .
Notez que ces points sont associés à la pression atmosphérique standard .
Radon – chaleur spécifique, chaleur latente de fusion, chaleur latente de vaporisation
La chaleur spécifique de radon est de 0,09 J / g K .
La chaleur latente de fusion du radon est de 2,89 kJ / mol .
La chaleur latente de vaporisation du radon est de 16,4 kJ / mol .
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: [email protected] ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci