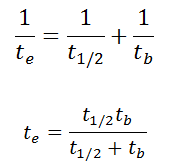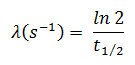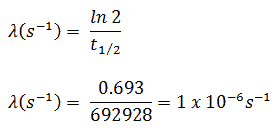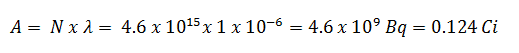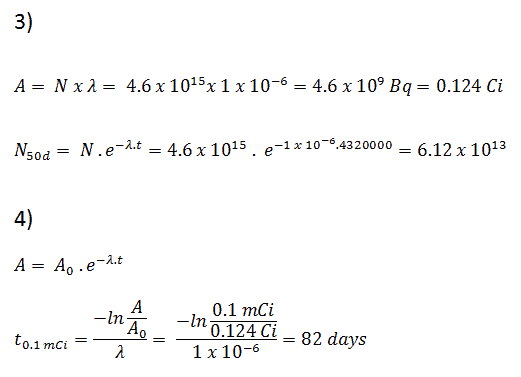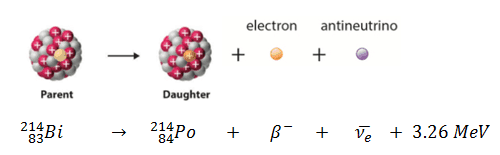Ley de descomposición – Ecuación – Fórmula
La ley de desintegración radiactiva establece que la probabilidad por unidad de tiempo de que un núcleo decaiga es una constante, independiente del tiempo. Esta constante se llama la constante de desintegración y se denota por λ, «lambda». Esta probabilidad constante puede variar mucho entre los diferentes tipos de núcleos, lo que lleva a las diferentes tasas de desintegración observadas. La desintegración radiactiva de cierto número de átomos (masa) es exponencial en el tiempo.
Ley de desintegración radiactiva: N = Ne -λt
La tasa de desintegración nuclear también se mide en términos de vidas medias . La vida media es la cantidad de tiempo que le toma a un isótopo dado perder la mitad de su radioactividad. Si un radioisótopo tiene una vida media de 14 días, la mitad de sus átomos se habrán descompuesto en 14 días. En 14 días más, la mitad de la mitad restante se descompondrá, y así sucesivamente. Las vidas medias varían desde millonésimas de segundo para productos de fisión altamente radiactivos hasta miles de millones de años para materiales de larga duración (como el uranio natural). Darse cuenta delas vidas medias cortas van con grandes constantes de descomposición. El material radiactivo con una vida media corta es mucho más radiactivo (en el momento de la producción) pero obviamente perderá su radiactividad rápidamente. No importa qué tan larga o corta sea la vida media, después de que hayan pasado siete vidas medias, queda menos del 1 por ciento de la actividad inicial.
La ley de desintegración radiactiva se puede derivar también para cálculos de actividad o cálculos de masa de material radiactivo:
(Número de núcleos) N = Ne -λt (Actividad) A = Ae -λt (Masa) m = me -λt
, donde N (número de partículas) es el número total de partículas en la muestra, A (actividad total) es el número de desintegraciones por unidad de tiempo de una muestra radiactiva, m es la masa del material radiactivo restante.
Decadencia constante y vida media – Ecuación – Fórmula
En los cálculos de radioactividad, se debe conocer uno de los dos parámetros ( constante de desintegración o vida media ), que caracterizan la tasa de desintegración. Existe una relación entre la vida media (t 1/2 ) y la constante de desintegración λ. La relación puede derivarse de la ley de descomposición estableciendo N = ½ N o . Esto da:
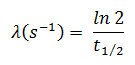 donde ln 2 (el logaritmo natural de 2) es igual a 0.693. Si se da la constante de desintegración (λ), es fácil calcular la vida media, y viceversa.
donde ln 2 (el logaritmo natural de 2) es igual a 0.693. Si se da la constante de desintegración (λ), es fácil calcular la vida media, y viceversa.
Ecuaciones de Bateman
En física, las ecuaciones de Bateman son un conjunto de ecuaciones diferenciales de primer orden, que describen la evolución en el tiempo de las concentraciones de nucleidos en cadena de desintegración lineal o en serie. El modelo fue formulado por Ernest Rutherford en 1905 y la solución analítica para el caso de desintegración radiactiva en una cadena lineal fue provista por Harry Bateman en 1910. Este modelo también se puede usar en códigos de agotamiento nuclear para resolver problemas de desintegración y transmutación nuclear.
Por ejemplo, ORIGEN es un sistema de código de computadora para calcular la acumulación, descomposición y procesamiento de materiales radiactivos. ORIGEN utiliza un método exponencial matricial para resolver un gran sistema de ecuaciones diferenciales ordinarias, de primer orden, acopladas, lineales (similares a las ecuaciones de Bateman ) con coeficientes constantes.
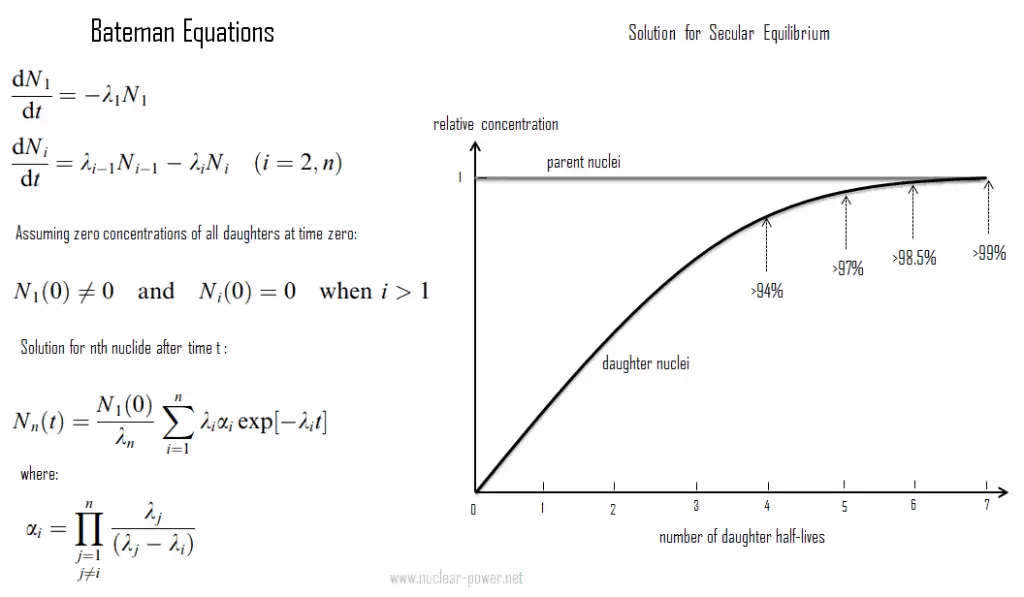
Las ecuaciones de Bateman para el caso de desintegración radiactiva de la serie n-nucleidos en cadena lineal que describe las concentraciones de nucleidos son las siguientes:
Ejemplo: Ley de descomposición radiactiva
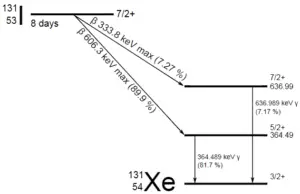 Una muestra de material contiene 1 microgramo de yodo-131. Tenga en cuenta que el yodo-131 desempeña un papel importante como isótopo radiactivo presente en los productos de fisión nuclear , y es un importante contribuyente a los riesgos para la salud cuando se libera a la atmósfera durante un accidente. El yodo 131 tiene una vida media de 8.02 días.
Una muestra de material contiene 1 microgramo de yodo-131. Tenga en cuenta que el yodo-131 desempeña un papel importante como isótopo radiactivo presente en los productos de fisión nuclear , y es un importante contribuyente a los riesgos para la salud cuando se libera a la atmósfera durante un accidente. El yodo 131 tiene una vida media de 8.02 días.
Calcular:
- El número de átomos de yodo-131 inicialmente presentes.
- La actividad del yodo-131 en curies.
- El número de átomos de yodo-131 que permanecerán en 50 días.
- El tiempo que le llevará a la actividad alcanzar 0.1 mCi.
Solución:
- El número de átomos de yodo-131 se puede determinar usando la masa isotópica como se muestra a continuación.
N I-131 = m I-131 . N A / M I-131
N I-131 = (1 μg) x (6.02 × 10 23 núcleos / mol) / (130.91 g / mol)
N I-131 = 4.6 x 10 15 núcleos
- La actividad del yodo-131 en los curies se puede determinar utilizando su constante de descomposición :
El yodo-131 tiene una vida media de 8.02 días (692928 segundos) y, por lo tanto, su constante de descomposición es:
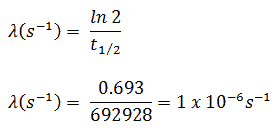
Usando este valor para la constante de desintegración podemos determinar la actividad de la muestra:
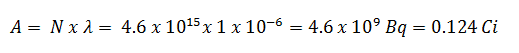
3) y 4) El número de átomos de yodo-131 que permanecerán en 50 días (N 50d ) y el tiempo que le tomará a la actividad alcanzar 0.1 mCi se puede calcular usando la ley de descomposición:
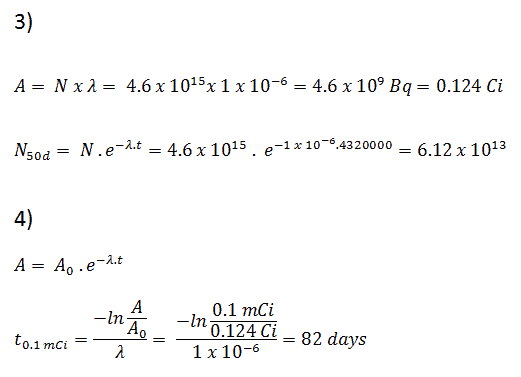
Como se puede ver, después de 50 días, el número de átomos de yodo-131 y, por lo tanto, la actividad será aproximadamente 75 veces menor. Después de 82 días, la actividad será aproximadamente 1200 veces menor. Por lo tanto, el tiempo de diez vidas medias (factor 2 10 = 1024) se usa ampliamente para definir la actividad residual.