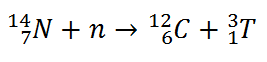Radionuclídeos cosmogênicos são radionuclídeos gerados pelas reações nucleares durante a interação entre raios cósmicos de alta energia e núcleos estáveis da atmosfera. Um dos radionuclídeos cosmogénicos bem conhecidos é o carbono-14, que é gerado pela reacção de 14 N (N, P) 14 C . Os outros isótopos gerados são os seguintes: 3 H, 7 Be, 22 Na. A maioria dos radionuclídeos cosmogênicos são produtos de (n, p), (p, n) e, especialmente, reações de fragmentação. Essas reações nucleares são muito rápidas e ocorrem em um período comparável ao tempo de trânsito de uma partícula incidente através do núcleo (~ 10-22s) O tempo de interação muito curto permite a interação de apenas um único núcleo (em casos extremos). Essas reações são conhecidas como reações nucleares diretas .
Carbono-14
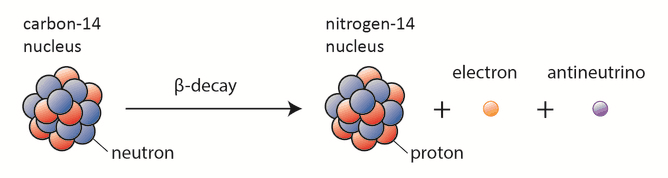
O único radionuclídeo cosmogênico que contribui significativamente para a exposição interna do ser humano é o carbono-14. O carbono radioativo-14 tem meia-vida de 5730 anos e sofre decaimento β , onde o nêutron é convertido em próton , elétron e antineutrino :
Apesar dessa meia-vida curta em comparação com a idade da Terra, o carbono-14 é um isótopo que ocorre naturalmente. Sua presença pode ser explicada pela seguinte observação simples. Nossa atmosfera contém muitos gases, incluindo o nitrogênio-14. Além disso, a atmosfera é constantemente bombardeada com raios cósmicos de alta energia , consistindo de prótons, núcleos mais pesados ou raios gama. Esses raios cósmicos interagem com os núcleos da atmosfera e também produzem nêutrons de alta energia . Esses nêutrons produzidos nessas colisões podem ser absorvidos pelo nitrogênio-14 para produzir um isótopo de carbono-14:
O carbono-14 também pode ser produzido na atmosfera por outras reações de nêutrons, incluindo em particular 13C (n, γ) 14C e 17O (n, α) 14C. Como resultado, o carbono-14 é formado continuamente na atmosfera superior pela interação dos raios cósmicos com o nitrogênio atmosférico. Em média, apenas um em cada 1,3 x 10 12 átomos de carbono na atmosfera é um átomo de carbono-14 radioativo. Como resultado, todas as substâncias biológicas vivas contêm a mesma quantidade de C-14 por grama de carbono, ou seja, 0,3 Bq de atividade do carbono-14 por grama de carbono. O carbono-14 está presente no corpo humano (13 kg de carbono em 70 kg humano) a um nível de cerca de 3700 Bq (0,1 μCi) com uma meia-vida biológica de 40 dias. Observe que meia-vida biológicaé o tempo necessário para que a quantidade de um elemento em particular no corpo diminua para metade do seu valor inicial devido à eliminação apenas por processos biológicos. No entanto, um átomo de carbono está na informação genética de cerca de metade das células, enquanto o potássio não é um componente do DNA. A decomposição de um átomo de carbono-14 no DNA de uma pessoa acontece cerca de 50 vezes por segundo, alterando um átomo de carbono para um de nitrogênio.
A dose anual de carbono-14 é estimada em cerca de 12 μSv / ano .
Enquanto o sistema biológico estiver vivo, o nível é constante devido à ingestão constante de todos os isótopos de carbono. Quando o sistema biológico morre, ele para de trocar carbono com o meio ambiente e, a partir desse momento, a quantidade de carbono-14 que ele contém começa a diminuir à medida que o carbono-14 sofre decaimento radioativo.
Veja também: Datação por carbono-14
Trítio
O trítio é o único radioisótopo de hidrogênio que ocorre naturalmente . Seu número atômico é naturalmente 1, o que significa que há 1 próton e 1 elétron na estrutura atômica. Ao contrário do núcleo de hidrogênio e núcleo de deutério, o trítio possui 2 nêutrons no núcleo. O trítio ocorre naturalmente, mas é extremamente raro .
O trítio é produzido na atmosfera quando os raios cósmicos colidem com as moléculas de ar. Na reação mais importante para a produção natural, um nêutron rápido (que deve ter energia superior a 4,0 MeV) interage com o nitrogênio atmosférico:
Em todo o mundo, a produção de trítio a partir de fontes naturais é de 148 petabecquerels por ano. Como resultado, a água tritiada produzida participa do ciclo da água.
- cerca de 400 Bq / m 3 em água continental
- cerca de 100 Bq / m 3 nos oceanos
O trítio é um isótopo radioativo, mas emite uma forma muito fraca de radiação, uma partícula beta de baixa energia que é semelhante a um elétron. É um emissor beta puro (ou seja, emissor beta sem uma radiação gama que o acompanha ). A energia cinética do elétron varia, com uma média de 5,7 keV, enquanto a energia restante é transportada pelo antineutrino do elétron quase indetectável . Uma energia tão baixa de elétrons causa que o elétron não pode penetrar na pele ou nem mesmo viaja muito longe no ar. As partículas beta do trítio podem penetrar apenas cerca de 6,0 mm de ar. O trítio decai por via beta negativa em hélio-3 com meia-vida de 12,3 anos .
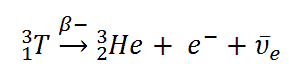 Portanto, o trítio representa um risco para a saúde como resultado da exposição interna somente após ingestão de água potável ou comida, inalação ou absorção pela pele. O trítio tomado no corpo é distribuído uniformemente entre todos os tecidos moles. Uma dose média anual da ingestão natural de trítio é de 0,01 μSv .
Portanto, o trítio representa um risco para a saúde como resultado da exposição interna somente após ingestão de água potável ou comida, inalação ou absorção pela pele. O trítio tomado no corpo é distribuído uniformemente entre todos os tecidos moles. Uma dose média anual da ingestão natural de trítio é de 0,01 μSv .
No caso de ingestão ou inalação artificial de trítio, um intervalo biológico de trítio é de 10 dias para o HTO e 40 dias para o OBT (trítio ligado organicamente) formado a partir do HTO no corpo de adultos. Também foi demonstrado que o intervalo biológico do HTO depende fortemente de muitas variáveis e varia de cerca de 4 a 18 dias. Durante os meses mais quentes, a meia-vida média é menor, o que é atribuído ao aumento da ingestão de água. Além disso, beber grandes quantidades de álcool reduzirá a meia-vida biológica da água no corpo.
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: translations@nuclear-power.com ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.