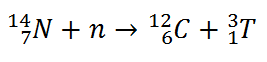Kosmogene Radionuklide sind Radionuklide, die durch Kernreaktionen während der Wechselwirkung zwischen energiereichen kosmischen Strahlen und stabilen Kernen aus der Atmosphäre erzeugt werden. Eines der bekannten kosmogenen Radionuklide ist Kohlenstoff-14, der durch die Reaktion 14 N (n, p) 14 C erzeugt wird . Die anderen erzeugten Isotope sind wie folgt: 3 H, 7 Be, 22 Na. Die meisten kosmogenen Radionuklide sind Produkte von (n, p), (p, n) und insbesondere Spallationsreaktionen. Diese Kernreaktionen sind sehr schnell und finden in einer Zeit statt, die mit der Transitzeit eines einfallenden Partikels durch den Kern vergleichbar ist (~ 10 -22)s). Die sehr kurze Wechselwirkungszeit ermöglicht nur die Wechselwirkung eines einzelnen Nukleons (in extremen Fällen). Diese Reaktionen werden als direkte Kernreaktionen bezeichnet .
Kohlenstoff-14
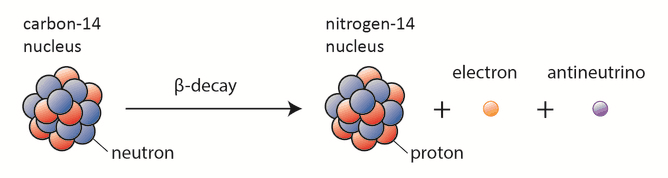
Das einzige kosmogene Radionuklid, das einen signifikanten Beitrag zur inneren Exposition des Menschen leistet, ist Kohlenstoff-14. Radioaktiver Kohlenstoff-14 hat eine Halbwertszeit von 5730 Jahren und unterliegt einem β− -Zerfall , bei dem das Neutron in ein Proton , ein Elektron und ein Elektron-Antineutrino umgewandelt wird :
Trotz dieser im Vergleich zum Alter der Erde kurzen Halbwertszeit ist Kohlenstoff-14 ein natürlich vorkommendes Isotop. Ihre Anwesenheit kann durch die folgende einfache Beobachtung erklärt werden. Unsere Atmosphäre enthält viele Gase, einschließlich Stickstoff-14. Außerdem wird die Atmosphäre ständig mit energiereichen kosmischen Strahlen bombardiert , die aus Protonen, schwereren Kernen oder Gammastrahlen bestehen. Diese kosmischen Strahlen interagieren mit Kernen in der Atmosphäre und produzieren auch energiereiche Neutronen . Diese Neutronen, die bei diesen Kollisionen entstehen, können von Stickstoff-14 absorbiert werden, um ein Isotop von Kohlenstoff-14 zu erzeugen:
Kohlenstoff-14 kann auch durch andere Neutronenreaktionen in der Atmosphäre erzeugt werden, einschließlich insbesondere 13C (n, γ) 14C und 17O (n, α) 14C. Infolgedessen wird Kohlenstoff-14 in der oberen Atmosphäre kontinuierlich durch Wechselwirkung kosmischer Strahlen mit atmosphärischem Stickstoff gebildet. Durchschnittlich ist nur eines von 1,3 × 10 12 Kohlenstoffatomen in der Atmosphäre ein radioaktives Kohlenstoff-14-Atom. Infolgedessen enthalten alle lebenden biologischen Substanzen die gleiche Menge an C-14 pro Gramm Kohlenstoff, dh 0,3 Bq Kohlenstoff-14-Aktivität pro Gramm Kohlenstoff. Kohlenstoff-14 ist im menschlichen Körper in einer Menge von etwa 3700 Bq (0,1 μCi) mit einer biologischen Halbwertszeit von 40 Tagen vorhanden (13 kg Kohlenstoff bei 70 kg Menschen). Beachten Sie, dass die biologische Halbwertszeitist die Zeit, die benötigt wird, um die Menge eines bestimmten Elements im Körper auf die Hälfte seines ursprünglichen Werts zu senken, und zwar allein aufgrund der Beseitigung durch biologische Prozesse. Ein Kohlenstoffatom ist jedoch in der genetischen Information von etwa der Hälfte der Zellen enthalten, während Kalium kein Bestandteil der DNA ist. Der Zerfall eines Kohlenstoff-14-Atoms in der DNA bei einer Person geschieht ungefähr 50 Mal pro Sekunde, wobei ein Kohlenstoffatom in Stickstoff umgewandelt wird.
Die jährliche Dosis von Kohlenstoff-14 wird auf etwa 12 μSv / Jahr geschätzt .
Solange das biologische System lebt, ist der Spiegel aufgrund der konstanten Aufnahme aller Kohlenstoffisotope konstant. Wenn das biologische System stirbt, hört es auf, Kohlenstoff mit seiner Umgebung auszutauschen, und von diesem Zeitpunkt an beginnt die Menge an Kohlenstoff-14, die es enthält, abzunehmen, wenn der Kohlenstoff-14 einem radioaktiven Zerfall unterliegt.
Siehe auch: Kohlenstoff-14-Datierung
Tritium
Tritium ist das einzige natürlich vorkommende Radioisotop von Wasserstoff. Seine Ordnungszahl ist natürlich 1, was bedeutet, dass sich 1 Proton und 1 Elektron in der Atomstruktur befinden. Im Gegensatz zum Wasserstoffkern und Deuteriumkern hat Tritium 2 Neutronen im Kern. Tritium ist natürlich vorkommend, aber äußerst selten .
Tritium entsteht in der Atmosphäre, wenn kosmische Strahlen mit Luftmolekülen kollidieren. Bei der wichtigsten Reaktion für die natürliche Produktion interagiert ein schnelles Neutron (das eine Energie von mehr als 4,0 MeV haben muss) mit Luftstickstoff:
Weltweit werden 148 Petabecquerel pro Jahr aus natürlichen Quellen produziert. Infolgedessen nimmt das erzeugte tritiierte Wasser am Wasserkreislauf teil.
- ca. 400 Bq / m 3 in kontinentalem Wasser
- etwa 100 Bq / m 3 in Ozeanen
Tritium ist ein radioaktives Isotop, emittiert jedoch eine sehr schwache Form von Strahlung, ein energiearmes Beta-Teilchen , das einem Elektron ähnlich ist. Es ist ein reiner Beta-Emitter (dh Beta-Emitter ohne begleitende Gammastrahlung ). Die kinetische Energie des Elektrons variiert mit durchschnittlich 5,7 keV, während die verbleibende Energie vom nahezu nicht nachweisbaren Elektronenantineutrino abgeführt wird . Eine so sehr niedrige Elektronenenergie führt dazu, dass das Elektron die Haut nicht durchdringen kann oder sich in der Luft nicht sehr weit bewegt. Beta-Partikel aus Tritium können nur etwa 6,0 mm Luft durchdringen. Tritium zerfällt durch negativen Beta-Zerfall in Helium-3 mit einer Halbwertszeit von 12,3 Jahren .
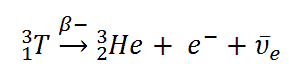 Daher stellt Tritium ein Gesundheitsrisiko dar, wenn es nur nach Einnahme in Trinkwasser oder Nahrung oder Einatmen oder Absorption durch die Haut einer inneren Exposition ausgesetzt wird. Das in den Körper aufgenommene Tritium ist gleichmäßig auf alle Weichteile verteilt. Eine durchschnittliche jährliche Dosis aus der natürlichen Tritiumaufnahme beträgt 0,01 μSv .
Daher stellt Tritium ein Gesundheitsrisiko dar, wenn es nur nach Einnahme in Trinkwasser oder Nahrung oder Einatmen oder Absorption durch die Haut einer inneren Exposition ausgesetzt wird. Das in den Körper aufgenommene Tritium ist gleichmäßig auf alle Weichteile verteilt. Eine durchschnittliche jährliche Dosis aus der natürlichen Tritiumaufnahme beträgt 0,01 μSv .
Bei künstlicher Aufnahme oder Inhalation von Tritium beträgt die biologische Halbwertszeit von Tritium 10 Tage für HTO und 40 Tage für OBT (organisch gebundenes Tritium), das aus HTO im Körper von Erwachsenen gebildet wird. Es wurde auch gezeigt, dass die biologische Halbwertszeit von HTO stark von vielen Variablen abhängt und zwischen 4 und 18 Tagen variiert. In den wärmeren Monaten ist die durchschnittliche Halbwertszeit niedriger, was auf eine erhöhte Wasseraufnahme zurückzuführen ist. Darüber hinaus verringert das Trinken größerer Mengen Alkohol die biologische Halbwertszeit von Wasser im Körper.
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: [email protected] oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.