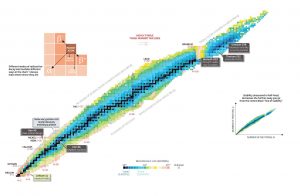
 Estabilidade nuclear é um conceito que ajuda a identificar a estabilidade de um isótopo. Para identificar a estabilidade de um isótopo, é necessário encontrar a proporção de nêutrons para prótons. Para determinar a estabilidade de um isótopo, você pode usar a razão nêutron / próton (N / Z). Também para ajudar a entender esse conceito, existe um gráfico dos nuclídeos, conhecido como gráfico de Segre. Este gráfico mostra um gráfico dos nuclídeos conhecidos em função de seus números atômicos e de nêutrons. Pode-se observar no gráfico que existem mais nêutrons do que prótons em nuclídeos com Z maior que cerca de 20 (cálcio). Esses nêutrons extras são necessários para a estabilidade dos núcleos mais pesados. O excesso de nêutrons age como uma cola nuclear.Veja também: Livechart – iaea.org
Estabilidade nuclear é um conceito que ajuda a identificar a estabilidade de um isótopo. Para identificar a estabilidade de um isótopo, é necessário encontrar a proporção de nêutrons para prótons. Para determinar a estabilidade de um isótopo, você pode usar a razão nêutron / próton (N / Z). Também para ajudar a entender esse conceito, existe um gráfico dos nuclídeos, conhecido como gráfico de Segre. Este gráfico mostra um gráfico dos nuclídeos conhecidos em função de seus números atômicos e de nêutrons. Pode-se observar no gráfico que existem mais nêutrons do que prótons em nuclídeos com Z maior que cerca de 20 (cálcio). Esses nêutrons extras são necessários para a estabilidade dos núcleos mais pesados. O excesso de nêutrons age como uma cola nuclear.Veja também: Livechart – iaea.org

Fonte: Livechart – IAEA.org
Os núcleos atômicos consistem em prótons e nêutrons, que se atraem através da força nuclear , enquanto os prótons se repelem através da força elétrica devido à sua carga positiva. Essas duas forças competem, levando a várias estabilidade dos núcleos. Existem apenas certas combinações de nêutrons e prótons, que formam núcleos estáveis .
Os nêutrons estabilizam o núcleo , porque se atraem e prótons, o que ajuda a compensar a repulsão elétrica entre os prótons. Como resultado, à medida que o número de prótons aumenta, é necessária uma proporção crescente de nêutrons para prótons para formar um núcleo estável. Se houver muitos ou poucos nêutrons para um dado número de prótons, o núcleo resultante não é estável e sofre decaimento radioativo . Isótopos instáveis decaem através de várias vias de decaimento radioativo, mais comumente decaimento alfa, decaimento beta ou captura de elétrons. Muitos outros tipos raros de deterioração, como fissão espontânea ou emissão de nêutrons, são conhecidos. Note-se que todas essas vias de decaimento podem ser acompanhadas pela emissão subsequente deradiação gama . Decaimentos alfa ou beta puros são muito raros.
Estabilidade Nuclear – Tabela Periódica
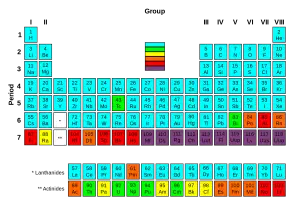
Dos 82 primeiros elementos da tabela periódica, 80 têm isótopos considerados estáveis. O tecnécio, o promécio e todos os elementos com um número atômico acima de 82 são instáveis e se decompõem por meio de decomposição radioativa. Não se espera que elementos pesados não descobertos (com número atômico acima de 110) sejam estáveis; portanto, o chumbo é considerado o elemento estável mais pesado. Para cada um dos 80 elementos estáveis, é fornecido o número de isótopos estáveis. Por exemplo, o estanho possui 10 desses isótopos estáveis.
Existem 80 elementos com pelo menos um isótopo estável, mas 114 a 118 elementos químicos são conhecidos. Todos os elementos do elemento 98 são encontrados na natureza e o restante dos elementos descobertos é produzido artificialmente, com todos os isótopos conhecidos por serem altamente radioativos com meias-vidas relativamente curtas.
Bismuto, tório, urânio e plutônio são nuclídeos primordiais porque têm meia-vida longa o suficiente para serem encontrados na Terra, enquanto todos os outros são produzidos por decaimento radioativo ou sintetizados em laboratórios e reatores nucleares . Nuclídeos primordiais são nuclídeos encontrados na Terra que existem em sua forma atual desde antes da formação da Terra. Nuclídeos primordiais são resíduos do Big Bang, de fontes cosmogênicas e de antigas explosões de supernovas que ocorreram antes da formação do sistema solar. Apenas 288 desses nuclídeos são conhecidos.
Conexão entre estabilidade nuclear e decaimento radioativo
Os núcleos dos radioisótopos são instáveis. Numa tentativa de alcançar uma disposição mais estável dos seus neutrões e os protões, o núcleo instável vai espontaneamente decair para formar um núcleo diferente. Se o número de nêutrons mudar no processo (o número de prótons permanece), um isótopo diferente é formado e um elemento permanece (por exemplo, emissão de nêutrons). Se o número de prótons mudar (número atômico diferente) no processo, um átomo de um elemento diferente é formado. Essa decomposição do núcleo é chamada de decaimento radioativo. Durante o decaimento radioativo, um núcleo instável decompõe-se espontaneamente e aleatoriamenteformar um núcleo diferente (ou um estado de energia diferente – decaimento gama), emitindo radiação na forma de partículas atômicas ou raios de alta energia. Esse decaimento ocorre a uma taxa constante e previsível, denominada meia-vida. Um núcleo estável não sofrerá esse tipo de decaimento e, portanto, não será radioativo.
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: [email protected] ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.