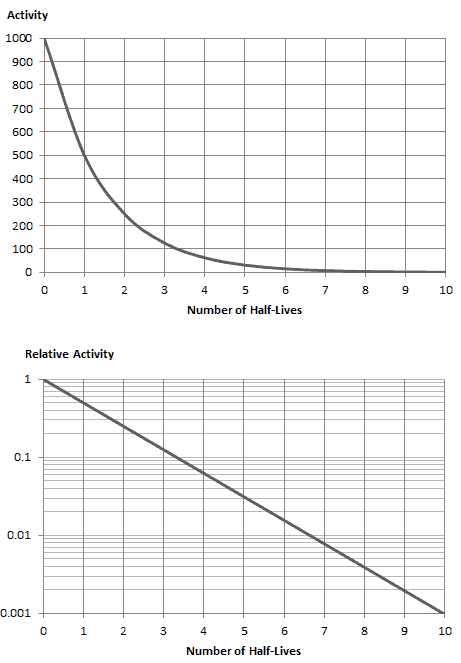
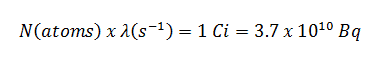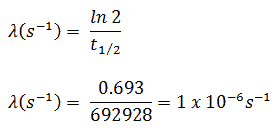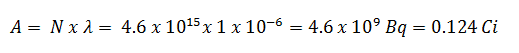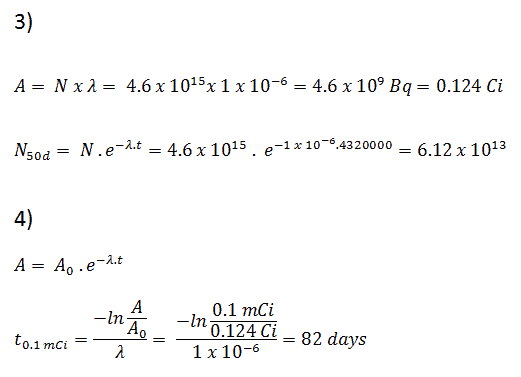A lei de decaimento radioativo afirma que a probabilidade por unidade de tempo que um núcleo decairá é uma constante, independente do tempo. Essa constante é chamada constante de decaimento e é denotada por λ, “lambda”. Essa probabilidade constante pode variar muito entre os diferentes tipos de núcleos, levando a muitas taxas diferentes de decaimento observadas. O decaimento radioativo de certo número de átomos (massa) é exponencial no tempo.
Lei de decaimento radioativo: N = Ne- λt
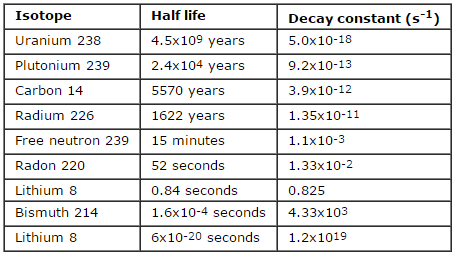
A taxa de decaimento nuclear também é medida em termos de meia-vida . A meia-vida é a quantidade de tempo que um determinado isótopo leva para perder metade de sua radioatividade. Se um radioisótopo tiver meia-vida de 14 dias, metade de seus átomos terá decaimento em 14 dias. Em mais 14 dias, metade da metade restante decairá e assim por diante. As meias-vidas variam de milionésimos de segundo para produtos de fissão altamente radioativos a bilhões de anos para materiais de longa duração (como o urânio que ocorre naturalmente). Notar quemeia-vida curta acompanha grandes constantes de decaimento. O material radioativo com meia-vida curta é muito mais radioativo (no momento da produção), mas obviamente perderá sua radioatividade rapidamente. Não importa quanto tempo a meia-vida seja curta ou curta, depois que sete meias-vidas tiverem passado, resta menos de 1% da atividade inicial.
A lei de decaimento radioativo também pode ser derivada para cálculos de atividade ou massa de cálculos de material radioativo:
(Número de núcleos) N = Ne -λt (Atividade) A = Ae -λt (Massa) m = me -λt
, onde N (número de partículas) é o número total de partículas na amostra, A (atividade total) é o número de decaimentos por unidade de tempo de uma amostra radioativa, m é a massa do material radioativo restante.
Decaimento constante e meia-vida
Nos cálculos de radioatividade, um dos dois parâmetros ( constante de decaimento ou meia-vida ), que caracterizam a taxa de decaimento, deve ser conhecido. Existe uma relação entre a meia-vida (t 1/2 ) e a constante de decaimento λ. O relacionamento pode ser derivado da lei de decaimento, definindo N = ½ N o . Isto dá:
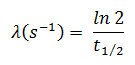 onde ln 2 (o logaritmo natural de 2) é igual a 0,693. Se a constante de decaimento (λ) for dada, é fácil calcular a meia-vida e vice-versa.
onde ln 2 (o logaritmo natural de 2) é igual a 0,693. Se a constante de decaimento (λ) for dada, é fácil calcular a meia-vida e vice-versa.
Constante de decaimento e radioatividade
A relação entre a meia-vida e a quantidade de radionuclídeo necessária para gerar uma atividade de um curie é mostrada na figura. Essa quantidade de material pode ser calculada usando λ , que é a constante de decaimento de determinado nuclídeo:
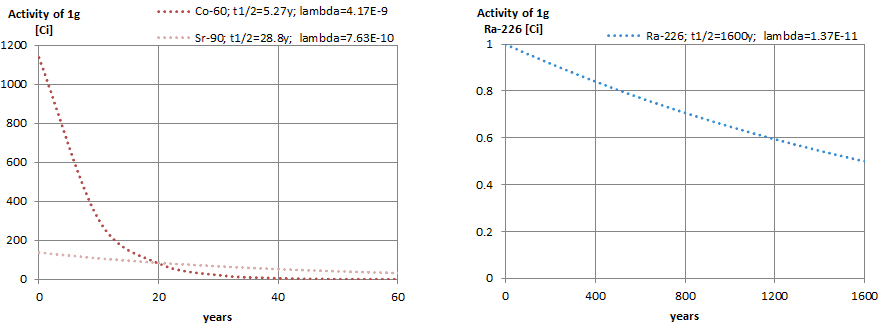
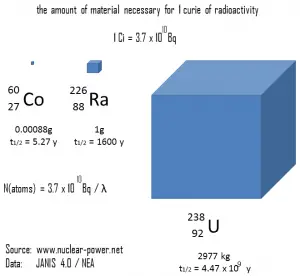 A figura a seguir ilustra a quantidade de material necessário para 1 curie de radioatividade. É óbvio que quanto maior a meia-vida, maior a quantidade de radionuclídeo necessária para produzir a mesma atividade. Evidentemente, a substância de vida mais longa permanecerá radioativa por muito mais tempo. Como pode ser visto, a quantidade de material necessário para 1 curie de radioatividade pode variar de uma quantidade muito pequena para ser vista (0,00088 grama de cobalto-60), através de 1 grama de rádio-226, a quase três toneladas de urânio-238 .
A figura a seguir ilustra a quantidade de material necessário para 1 curie de radioatividade. É óbvio que quanto maior a meia-vida, maior a quantidade de radionuclídeo necessária para produzir a mesma atividade. Evidentemente, a substância de vida mais longa permanecerá radioativa por muito mais tempo. Como pode ser visto, a quantidade de material necessário para 1 curie de radioatividade pode variar de uma quantidade muito pequena para ser vista (0,00088 grama de cobalto-60), através de 1 grama de rádio-226, a quase três toneladas de urânio-238 .
Exemplo – Cálculo de Radioatividade
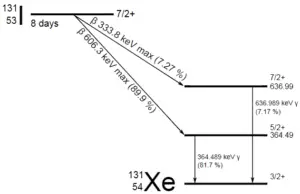 Uma amostra de material contém 1 micrograma de iodo-131. Observe que o iodo-131 desempenha um papel importante como isótopo radioativo presente nos produtos de fissão nuclear e é um dos principais contribuintes para os riscos à saúde quando liberado na atmosfera durante um acidente. O iodo-131 tem uma meia-vida de 8,02 dias.
Uma amostra de material contém 1 micrograma de iodo-131. Observe que o iodo-131 desempenha um papel importante como isótopo radioativo presente nos produtos de fissão nuclear e é um dos principais contribuintes para os riscos à saúde quando liberado na atmosfera durante um acidente. O iodo-131 tem uma meia-vida de 8,02 dias.
Calcular:
- O número de átomos de iodo-131 inicialmente presentes.
- A atividade do iodo-131 nos curies.
- O número de átomos de iodo-131 que permanecerá em 50 dias.
- O tempo necessário para a atividade atingir 0,1 mCi.
Solução:
- O número de átomos de iodo-131 pode ser determinado usando a massa isotópica como abaixo.
N -131 = m I-131 . N A / H I-131
NI -131 = (1 μg) x (6,02 × 10 23 núcleos / mol) / (130,91 g / mol)
NI -131 = 4,6 x 10 15 núcleos
- A atividade do iodo-131 em curies pode ser determinada usando sua constante de decaimento :
O iodo-131 tem meia-vida de 8,02 dias (692928 seg) e, portanto, sua constante de decaimento é:
Usando esse valor para a constante de decaimento, podemos determinar a atividade da amostra:
3) e 4) O número de átomos de iodo-131 que permanecerá em 50 dias (N 50d ) e o tempo necessário para a atividade atingir 0,1 mCi podem ser calculados usando a lei de decaimento:
Como pode ser visto, após 50 dias o número de átomos de iodo-131 e, portanto, a atividade será cerca de 75 vezes menor. Após 82 dias, a atividade será aproximadamente 1200 vezes menor. Portanto, o tempo de dez meias-vidas (fator 2 10 = 1024) é amplamente utilizado para definir a atividade residual.
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: [email protected] ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.