Radon ist ein farbloses, geruchloses, geschmackloses Edelgas , das auf natürliche Weise als Zerfallsprodukt von Radium vorkommt. Radon ist ein chemisches Element mit der Ordnungszahl 86 , das bedeutet , dass es 86 Protonen und 86 Elektronen in der Atomstruktur ist. Das chemische Symbol für Radon ist Rn . Alle Radonisotope sind radioaktiv , aber die beiden Radonisotope Radon-222 und Radon-220 sind aus Strahlenschutzgründen sehr wichtig.
-
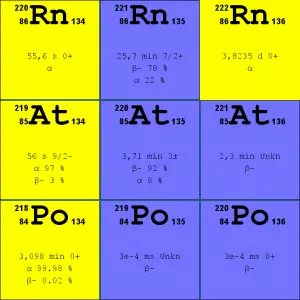
Quelle: JANIS (Java-basierte Nuclear Data Information Software); ENDF / B-VII.1 Radon-222 . Das Radon-222-Isotop ist ein natürliches Zerfallsprodukt des stabilsten Uranisotops (Uran-238) und gehört daher zur Uranreihe .
- Radon-220 . Das Radon-220-Isotop, das allgemein als Thoron bezeichnet wird , ist ein natürliches Zerfallsprodukt des stabilsten Thoriumisotops ( Thorium-232 ) und gehört daher zur Thoriumreihe .
Es ist wichtig anzumerken, dass Radon ein Edelgas ist , während alle seine Zerfallsprodukte Metalle sind . Der Hauptmechanismus für den Eintritt von Radon in die Atmosphäre ist die Diffusion durch den Boden . Radon diffundiert als Gas durch Gesteine und den Boden. Wenn Radon zerfällt, sind die metallischen Isotope der Tochter Ionen, die an andere Moleküle wie Wasser und Aerosolpartikel in der Luft gebunden werden. Daher beziehen sich alle Diskussionen über Radonkonzentrationen in der Umwelt auf Radon-222. Während die durchschnittliche Produktionsrate von Radon-220 (Thoron) in etwa der von Radon-222 entspricht, ist die Menge an Radon-220 in der Umwelt aufgrund der signifikant kürzeren Halbwertszeit viel geringer als die von Radon-222 ( Es hat weniger Zeit, Radon-222 zu verbreiten (55 Sekunden gegenüber 3,8 Tagen). Radon-220 hat einfach eine geringere Chance, aus dem Gestein zu entkommen.
Siehe auch: Radon – Gesundheitliche Auswirkungen
Radon – Eigenschaften
| Element | Radon |
|---|---|
| Ordnungszahl | 86 |
| Symbol | Rn |
| Elementkategorie | Edelgas |
| Phase bei STP | Gas |
| Atommasse [amu] | 222 |
| Dichte bei STP [g / cm3] | 9.73 |
| Elektronenkonfiguration | [Hg] 6p6 |
| Mögliche Oxidationszustände | 0 |
| Elektronenaffinität [kJ / mol] | – – |
| Elektronegativität [Pauling-Skala] | – – |
| 1. Ionisierungsenergie [eV] | 10.7485 |
| Jahr der Entdeckung | 1900 |
| Entdecker | Dorn, Friedrich Ernst |
| Thermische Eigenschaften | |
| Schmelzpunkt [Celsius-Skala] | -71 |
| Siedepunkt [Celsius-Skala] | -61,8 |
| Wärmeleitfähigkeit [W / m K] | 0,00361 |
| Spezifische Wärme [J / g K] | 0,09 |
| Schmelzwärme [kJ / mol] | 2.89 |
| Verdampfungswärme [kJ / mol] | 16.4 |
Atommasse von Radon
Die Atommasse von Radon beträgt 222 u.
Es ist zu beachten, dass jedes Element mehr Isotope enthalten kann, daher wird diese resultierende Atommasse aus natürlich vorkommenden Isotopen und ihrer Häufigkeit berechnet.
Die Maßeinheit für die Masse ist die Atommasseneinheit (amu) . Eine Atommasseneinheit entspricht 1,66 x 10 -24 Gramm. Eine einheitliche Atommasseneinheit ist ungefähr die Masse eines Nukleons (entweder ein einzelnes Proton oder ein Neutron) und entspricht numerisch 1 g / mol.
Dichte von Radon
Die Radondichte beträgt 9,73 g / cm 3 .

Typische Dichten verschiedener Substanzen bei atmosphärischem Druck.
Die Dichte ist definiert als die Masse pro Volumeneinheit . Es ist eine intensive Eigenschaft , die mathematisch definiert ist als Masse geteilt durch Volumen:
ρ = m / V.
Mit anderen Worten, die Dichte (ρ) einer Substanz ist die Gesamtmasse (m) dieser Substanz geteilt durch das Gesamtvolumen (V), das von dieser Substanz eingenommen wird. Die Standard-SI-Einheit ist Kilogramm pro Kubikmeter ( kg / m 3 ). Die englische Standardeinheit ist Pfund Masse pro Kubikfuß ( lbm / ft 3 ).
Siehe auch: Was ist Dichte?
Siehe auch: Dichteste Materialien der Erde
Radon – Schmelzpunkt und Siedepunkt
Schmelzpunkt von Radon ist -71 ° C .
Siedepunkt von Radon ist -61,8 ° C .
Beachten Sie, dass diese Punkte dem normalen atmosphärischen Druck zugeordnet sind .
Radon – spezifische Wärme, latente Schmelzwärme, latente Verdampfungswärme
Spezifische Wärme von Radon ist 0,09 J / g K .
Die latente Schmelzwärme von Radon beträgt 2,89 kJ / mol .
Die latente Verdampfungswärme von Radon beträgt 16,4 kJ / mol .
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: [email protected] oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.